��Ŀ����
18��ij��ѧ�С��������Fe��Al������Ե�ǿ������ͬѧѡ��1mol•L-1�����ᣮ��ͬѧѡ��18.4mol•L-1�����ᣮ��ͬѧ��Fe��Alֱ�Ӳ���1mol•L-1�������У�����Fe��Al�����ӣ�Fe��Al���Ͼ������ݷų��������ӵ�����������FeΪ������AlΪ��������ͬѧ��Fe��Alֱ�Ӳ���18.4mol•L-1�������У�����Fe��Al�����ӣ�Fe��Al���������Ա仯�����ӵ�������������ʾ��Ϊ0����1����д����ͬѧ����ʵ���У�Fe��Al���ӵ�����ʱ��������Ӧ���ܻ�ѧ����ʽ��2Al+3H2SO4�T2Al2��SO4��3+3H2����
����ͬѧ�۲쵽������ʾ��Ϊ0��ԭ������������Ũ�����лᷢ���ۻ��������γ��Է���������ԭ��Ӧ��
�ۼ�ͬѧ���ý��������Ľ�����Ա���ǿ
��2����֪�����£�A1��0H��3��Ksp=3.2��10-34�����¶����������ʵ��ķ�Һ�м���NaOH��Һ��pH=5�����жϸ��¶���Al3+�Ƿ������ȫ���ǣ���ǡ�������ʱ��Һ�е�Al3+��Ũ��Ϊ3.2��10-7mol/L��
���� ��1����Fe��Al���ӵ�����ʱ������Ϊ��������Ϊ�����缫��ӦΪ�������ᷴӦ������������������
��18.4mol•L-1������ΪŨ���ᣬ��������Ũ�����лᷢ���ۻ��������γ�ԭ��أ�
�ۼ�ͬѧ����ʵ���У����������Ӻ���Ϊ��������Ϊ������֤�����Ļ����Խ�ǿ��
��2�������pH=5ʱ��Һ������������Ũ�ȣ�Ȼ����ݸ���Ksp=c3��OH-����c��Al3+�� ���������Һ��������Ũ�ȣ��ٸ��ݼ������ж��������Ƿ������ȫ��
��� �⣺��1����Fe��Al���ӵ�����ʱ������ΪAl������ΪFe��������ʧȥ���ӣ����������ӵõ����ӣ��缫�ܷ�ӦΪ��2Al+3H2SO4�T2Al2��SO4��3+3H2����
�ʴ�Ϊ��2Al+3H2SO4�T2Al2��SO4��3+3H2����
�ڽ�Fe��Alֱ�Ӳ���18.4mol•L-1�������У�������ΪŨ���ᣬ��������Ũ�����лᷢ���ۻ��������γ��Է���������ԭ��Ӧ������û���γ�ԭ��أ���۲쵽������ʾ��Ϊ0��
�ʴ�Ϊ����������Ũ�����лᷢ���ۻ��������γ��Է���������ԭ��Ӧ��
�ۼ�ͬѧ��Fe��Al���ӵ�����ʱ������ΪAl������ΪFe��������ʧȥ���ӣ����������ӵõ����ӣ�˵�����Ľ�����Ա���ǿ��
�ʴ�Ϊ�����Ľ�����Ա���ǿ��
��2��������pH=5ʱ֪c��OH-��=10-9mol/L������Ksp=c3��OH-����c��Al3+�� ��֪��c��Al3+��=$\frac{3.2��1{0}^{-34}}{��{1��1{0}^{-9}��}^{3}}$mol/L=3.2��10-7mol/L��1��10-5mol/L���������ӳ�����ȫ��
�ʴ�Ϊ���ǣ�3.2��10-7mol/L��
���� ���⿼����ԭ��ع���ԭ�����������ܶȻ��ļ����֪ʶ����Ŀ�Ѷ��еȣ���ȷԭ��ع���ԭ��Ϊ���ؼ���ע�������������ܶȻ��ı���ʽ�����㷽��������������ѧ���ķ�����������ѧ����������

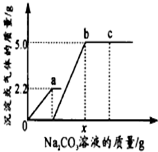 ��һ������CaCl2��HCl�Ļ����Һ����μ���������������Ϊ10%��Na2CO3��Һ����Ӧ�����м����Na2CO3��Һ����������������������������ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
��һ������CaCl2��HCl�Ļ����Һ����μ���������������Ϊ10%��Na2CO3��Һ����Ӧ�����м����Na2CO3��Һ����������������������������ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ͼ��oa�α�ʾ���ɳ����Ĺ��� | B�� | b����Һ��������2�� | ||
| C�� | c����Һ��pH=7 | D�� | xֵΪ106.0 |
| A�� | Cu2++2OH-�TCu��OH��2���� CuCO3+2NaOH�TCu��OH��2��+Na2CO3 | |
| B�� | CO32-+2H+�TCO2��+H2O�� BaCO3+2HCl�TBaCl2+CO2��+H2O | |
| C�� | Ca2++CO32-�TCaCO3���� Ca��NO3��2+Na2CO3�TCaCO3��+2NaNO3 | |
| D�� | H++OH-�TH2O�� 2KOH+H2SO4�TK2SO4+2H2O |
| A�� | ����ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2�� | |
| B�� | ̼��þ�����ᷴӦ��MgCO3+2H+=Mg2++CO2��+H2O | |
| C�� | ͭ����������Һ��Ӧ��Cu+Ag+=Cu2++Ag | |
| D�� | ����þ��Һ������������Һ��Ӧ��SO42-+Ba2+�TBaSO4�� |
| A�� | ����Ϊ��̿��������O2 | B�� | ����ΪAlCl3��������NaOH | ||
| C�� | ����ΪFe������������ | D�� | ����ΪNaOH ��Һ��������CO2 |