题目内容
11.关于卤素的下列叙述正确的是( )| A. | 卤素是典型的非金属元素,因此不能与其他非属元素化合 | |
| B. | 同周期中卤族元素的电负性最小 | |
| C. | 卤素各单质都能和水剧烈反应 | |
| D. | 卤素单质都能和H2反应,且气态氢化物的稳性随单质氧化性的增强而增强 |
分析 A.卤素具有强氧化性,能和其它非金属元素化合;
B.同一周期元素,电负性随着原子序数增大而增大;
C.卤素单质中只有氟气和水反应剧烈;
D.卤素非金属性随着原子序数增大而减弱,元素的非金属性越强,其氢化物的稳定性越强,其单质的氧化性越强,卤素单质氧化性较强.
解答 解:A.卤素能与其它非金属化合,如H、C、O等,故A错误;
B.同一周期元素,电负性随着原子序数增大而增大,所以卤素电负性最大,故B错误;
C.卤素单质中只有氟能与水剧烈反应生成氟化氢和氧气,故C错误;
D.卤素非金属性随着原子序数增大而减弱,元素的非金属性越强,其氢化物的稳定性越强,其单质的氧化性越强,卤素单质氧化性较强,所以卤素单质都能和H2反应,且气态氢化物的稳性随单质氧化性的增强而增强,故D正确;
故选D.
点评 本题考查卤族元素性质递变规律,卤族元素是电性的非金属元素,知道非金属性强弱与电负性、氢化物的稳定性、最高价氧化物的水化物酸性强弱关系,题目难度不大.

练习册系列答案
相关题目
1.1999年诺贝多尔化学状获得者艾哈迈德•泽维尔开创了“飞秒化学”的新领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能.你认为该技术不能观察到的是( )
| A. | 化学变化中反应物分子的分解 | B. | 反应中原子的运动 | ||
| C. | 化学变化中生成物分子的形成 | D. | 原子核的内部结构 |
16.下列分子或离子中,中心原子含有孤对电子的是( )
| A. | NH4+ | B. | CCl4 | C. | SiH4 | D. | H3P |
3.如图是恒温下某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( )
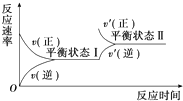

| A. | 反应达平衡时,正反应速率和逆反应速率相等 | |
| B. | 该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ | |
| C. | 该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ | |
| D. | 同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等 |
 在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“.请回答该实验中的问题.
在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“.请回答该实验中的问题.