题目内容
7.下列说法正确的是( )| A. | 明矾净水过程中不涉及化学变化 | B. | 金属与盐溶液反应都是置换反应 | ||
| C. | 化合反应一定有单质参加反应 | D. | 石油分馏和碘的升华都是物理变化 |
分析 A.明矾净水是明矾电离产生铝离子水解生成具有吸附性的氢氧化铝胶体;
B.有些属于化合反应,如氯化铁与铁的反应;
C.氨气与氯化氢反应生成氯化铵;
D.有新物质生成的变化属于化学变化.
解答 解:A.明矾净水是明矾电离产生铝离子水解生成具有吸附性的氢氧化铝胶体,该过程有新物质生成属于化学变化,故A错误;
B.金属与盐溶液反应不一定为置换反应,有些属于化合反应,如氯化铁与铁的反应,故B错误;
C.氨气与氯化氢反应生成氯化铵,该反应为化合反应,没有单质参加,故C错误;
D.石油分馏和碘的升华都没有新物质生成都是物理变化,故D正确;
故选:D.
点评 本题考查了物理变化、化学变化的区别,置换反应、化合反应的判断,明确过程有无新物质生成是判断化学变化、物理变化的根本依据,注意对置换反应、化合反应概念的理解,题目难度不大.

练习册系列答案
相关题目
17.25℃时,在pH=2的溶液中能大量共存的离子组是( )
| A. | Fe3+、Mg2+、SO42-、Cl- | B. | Ba2+、K+、I-、NO3- | ||
| C. | Fe2+、Cu2+、AlO2-、ClO- | D. | Na+、Ca2+、Cl-、CO32- |
15.在下列各溶液中,离子一定能大量共存的是( )
| A. | 室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42- | |
| B. | 含有0.1mol•L-1Fe3+的溶液中:K+、Mg2+、I-、NO3- | |
| C. | 无色溶液中:K+、Na+、MnO4-、SO42- | |
| D. | pH=11的溶液中:CO32-、Na+、AlO2-、NO3- |
12.下列有关双氧水说法错误的是( )
| A. | H2O2、Na2O2都属于过氧化物,都存在非极性共价键 | |
| B. | 1mol H2O2在参加反应时可能转移lmol或2mol电子 | |
| C. | H2O2在酶作用下催化分解,随着温度的升高,分解速率持续加快 | |
| D. | H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似、与SO2不同 |
19.把炭和氧化铜组成的混合物隔绝空气加热,充分反应后称量所得剩余固体的质量为112g,向此剩余固体中加入200g稀硫酸,稀硫酸恰好被完全反应,过滤后所得滤渣呈红色.同时将反应所得的气体全部通入含溶质37g的澄清石灰水中,得到沉淀25g.下列有关说法正确的是( )
| A. | 生成气体的质量可能是11克或33克 | |
| B. | 滤渣中的红色物质可能是32克或96克 | |
| C. | 参与反应的氧化铜质量可能是40克或120克 | |
| D. | 稀硫酸的溶质质量可能是38.4克或115.2克 |
16.下列实验误差分析错误的是( )
| A. | 用湿润的pH试纸测稀碱液的,测定值偏小 | |
| B. | 用量筒量取10mLNaOH 溶液时,俯视刻度.量出的体积大于10mL | |
| C. | 使用天平称量时不小心将药品与砝码的位置放反了,称最结果可能是准确的 | |
| D. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小 |
9.根据电解质在溶液中的电离情况,我们划分出了酸、碱、盐,通过学习我们知道酸和碱都有通性,而盐是没有通性的,其本质原因是( )
| A. | 盐不能电离出阳离子 | B. | 盐不能电离出阴离子 | ||
| C. | 盐不能电离出H+或OH- | D. | 盐不能电离出共同的离子 |

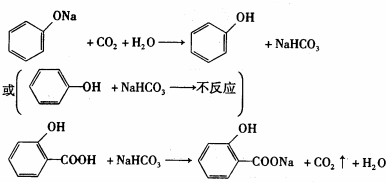 .
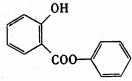
. ;反应类型:加成反应.
;反应类型:加成反应. ;反应类型:酯化反应
;反应类型:酯化反应