题目内容
加碘食盐中含有的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
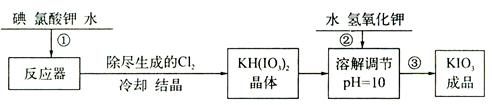
(1)步骤②中氢氧化钾的主要作用是 。
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,可经过 、过滤、洗涤、干燥等步骤。
(3)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2O32-=2I-+S4O62-
为了测定加碘食盐中碘的含量,某学生设计了如下实验:准确称取wg食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;最后加入指示剂,以物质的量浓度为2.00×10-3mol·L-1的Na2S2O3溶液滴定,消耗10.00mL时恰好反应完全。
在滴定过程中,所用的玻璃仪器为 、 。
该实验可以用 作指示剂,滴定终点的现象是 。
③ 下列有关该滴定实验的说法不正确的是 。
A.滴定管在使用前必须检查是否漏水并润洗 B.滴定时眼睛注视滴定管内溶液液面变化
C.为减小实验误差,可用少量的蒸馏水冲洗锥形瓶内壁 D.终点读数时俯视会导致碘的含量偏低
④加碘食盐样品中的碘元素含量是 g·kg-1(以含w的代数式表示)。

(1)步骤②中氢氧化钾的主要作用是 。
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,可经过 、过滤、洗涤、干燥等步骤。
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |
(3)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2O32-=2I-+S4O62-
为了测定加碘食盐中碘的含量,某学生设计了如下实验:准确称取wg食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;最后加入指示剂,以物质的量浓度为2.00×10-3mol·L-1的Na2S2O3溶液滴定,消耗10.00mL时恰好反应完全。
在滴定过程中,所用的玻璃仪器为 、 。
该实验可以用 作指示剂,滴定终点的现象是 。
③ 下列有关该滴定实验的说法不正确的是 。
A.滴定管在使用前必须检查是否漏水并润洗 B.滴定时眼睛注视滴定管内溶液液面变化
C.为减小实验误差,可用少量的蒸馏水冲洗锥形瓶内壁 D.终点读数时俯视会导致碘的含量偏低
④加碘食盐样品中的碘元素含量是 g·kg-1(以含w的代数式表示)。
(1)与KH(IO3)2反应使其转化为KIO3 (2)蒸发结晶
(3)① 碱式滴定管 锥形瓶 。② 淀粉溶液 溶液的蓝色消失且半分钟内不再变化 ③B ④1.27/3w
(3)① 碱式滴定管 锥形瓶 。② 淀粉溶液 溶液的蓝色消失且半分钟内不再变化 ③B ④1.27/3w
试题分析:(1)碘单质与氯酸钾在水中发生反应产生KH(IO3)2,加入KOH时可以使之转化为KIO3。(2)由于碘酸钾的溶解度受温度的影响变化不大,所以从KIO3溶液中得到晶体的操作方法是采用蒸发溶剂结晶、过滤、洗涤、干燥等步骤。(3)①由题意可知是用Na2S2O3溶液滴定I2的水溶液。Na2S2O3溶液显碱性所以在滴定过程中,所用的玻璃仪器为碱式滴定管和锥形瓶。②由于单质I2遇淀粉溶液显蓝色。所以可以利用淀粉溶液作指示剂。当达到滴定终点时现象是溶液的蓝色消失且半分钟内不再变化。③A滴定管在使用前必须检查是否漏水并润洗。正确。B滴定时眼睛要注视锥形瓶中溶液颜色的变化。错误。C.可用少量的蒸馏水冲洗锥形瓶内壁,扩大溶液的体积,可以使滴定过程中锥形瓶中物质的浓度减小,这样可以减小实验误差,提高实验的准确度。正确。D.终点读数时若俯视会导致滴定所用Na2S2O3溶液的体积偏小,以此为标准计算的碘的含量就偏低。正确。故有关该滴定实验的说法不正确的是B。④由方程式KIO3+5KI+3H2SO4= 3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-可得关系式KIO3—— 3I2 —— 6S2O32-.n(Na2S2O3)=2.00×10-5mol.所以n(KIO3)=1/3×10-5mol.所以碘元素的质量为1/3×10-5mol ×127g/mol =1.27/3×10-3g.所以该加碘食盐样品中的碘元素含量是1.27/3×10-3g÷w×10-3Kg=1.27/3w.

练习册系列答案
相关题目