题目内容
20g由两种金属粉末组成的混合物,与足量的盐酸反应后得倒11.2L氢气(标准状况下),这种金属混合物的组成可能是
| A.Mg和Al | B.Al和Fe | C.Fe和Zn | D.Zn和Cu |
B
足量的盐酸反应后得倒11.2L氢气即氢气的物质的量为0.5mol,若为镁则需质量为12g;若为AL则需质量为9g;若为铁则需质量为28g;若为锌则需质量为32.5g;若为铜不反应;由此可得,20g由两种金属粉末组成的混合物,与足量的盐酸反应后得倒11.2L氢气,这种金属混合物可能是Al和Fe ;

练习册系列答案
相关题目
 重要材料。研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究。填写下列空白。
重要材料。研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究。填写下列空白。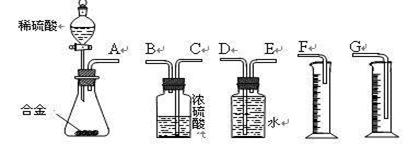
 相平
相平
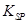 = 2.70×10-39]
= 2.70×10-39] Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡
Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡 酸钾溶液,观察溶液紫色是否褪色或变浅
酸钾溶液,观察溶液紫色是否褪色或变浅