题目内容
【题目】某稀溶液中含有等物质的量的ZnSO4、Fe2(SO4)3、H2SO4、CuSO4,向其中逐渐加入铁粉。下列各图表示溶液中Fe2+的物质的量和加入铁粉的物质的量之间的关系,其中可能正确的是( )
A.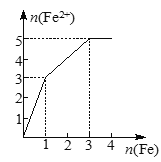 B.
B.
C. D.
D.
【答案】A
【解析】
向含有等物质的量的ZnSO4、Fe2(SO4)3、H2SO4、CuSO4的混合溶液中逐渐加入铁粉,铁粉和各离子反应的先后顺序是:铁离子、铜离子、氢离子(锌离子不与铁粉反应),涉及的反应方程式为:Fe2(SO4)3+Fe=3FeSO4、CuSO4+Fe=FeSO4+Cu、H2SO4+Fe=
FeSO4+H2↑,等物质的量的Fe2(SO4)3、H2SO4、CuSO4分别和等物质的量的铁完全反应生成硫酸亚铁,生成硫酸亚铁的物质的量之比是3:1:1,A正确,故答案为:A。

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目