题目内容
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。则下列说法正确的是( )
| A.电池工作时,MnO2发生还原反应 |
| B.电池负极的电极反应式为:2MnO2+H2O+2e-→Mn2O3+2OH- |
| C.电池工作时,K+移向负极 |
| D.电池工作时,电路中每通过0.1mol电子,锌的质量理论上减少6.5g |
A
解析试题分析:A.有电池的总反应方程式可知:电池工作时,Zn 失去电子,被氧化;而MnO2得到电子,发生还原反应,正确。B.电池负极的电极反应式为: Zn-2e-+2OH-→Zn(OH)2(s).错误。C.电池工作时,K+移向负电荷较多的正极。错误。D.电池工作时,电路中每通过0.1mol电子,锌的质量理论上减少3.25g.错误。
考点:考查锌-锰碱性电池的各种原理的知识。

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O===3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述正确的是( )
| A.放电时,负极反应式为3Zn-6e-+6OH-===3Zn(OH)2 |
| B.放电时,正极区溶液的pH减小 |
| C.充电时,每转移3 mol电子,阳极有1 mol Fe(OH)3被还原 |
| D.充电时,电池的锌电极接电源的正极 |
如图所示是利用电化学降解法治理水中的硝酸盐污染,电解槽中间用质子交换膜隔开,污水放入II区,通电使转NO3-化为N2,下面说法不正确的是 ( )
| A.电解时H+从I区通过离子交换膜迁移到II区 |
| B.Ag-Pt电极上发生发应:2 NO3-+10e-+6H2O= N2↑+12OH- |
| C.当电解过程中转移了1moL电子,则II区电解液质量减少2.8g |
| D.为增强溶液的导电性,I区水中可加入少量Na2SO4固体 |
如图装置,U形管中装有50 mL 2 mol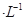 的CuSO4溶液。通电一段时间后,下列说法正确的是
的CuSO4溶液。通电一段时间后,下列说法正确的是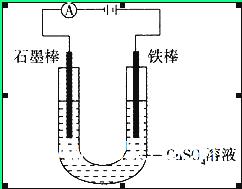
| A.转移0.2 mol电子时,阳极减少质量大于阴极增加质量 |
| B.转移0.4 mol电子时,阴极得到2.24 L标准状况下的气体 |
| C.电解一段时间后,U形管中会产生红褐色物质,后来逐渐溶解 |
| D.若将石墨棒换成铜棒,可实现铁制品上镀铜 |
下图是一种燃料型电池检测仪的工作原理示意图。下列说法不正确的是 ( )
| A.该仪器工作时酒精浓度越大,则电流强度越大 |
| B.工作时处电路电子流向为X→Y |
| C.检测结束后,X极区的pH增大 |
| D.电池总反应为2CH3CH2OH+O2=2CH3CHO+2H2O |
下列有关原电池的说法中,正确的是( )
| A.铝片和镁片用导线连接后插入NaOH溶液中,镁片较活泼,作负极 |
| B.铝片和铜片用导线连接后插入浓硝酸中,铜作负极 |
| C.镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀 |
| D.将反应2Fe3++Fe=3Fe2+设计为原电池,则可用锌片作负极,铁片作正极,FeCl3溶液作电解质 |
以Fe为阳极,Pt为阴极,对足量的 Na2SO4 溶液进行电解,一段时间后得到4 mol Fe(OH)3沉淀,此间共消耗水的物质的量为 ( )
| A.6mol | B.8mol | C.10mol | D.12mol |
(2014?长宁区一模)①②③④甲种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活泼性由大到小的顺序是( )
| A.①③②④ | B.①③④② | C.③④②① | D.③①②④ |
下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是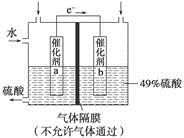
| A.该装置将化学能转化为电能 |
| B.催化剂b表面O2发生还原反应,其附近酸性增强 |
| C.催化剂a表面的反应是SO2+2H2O-2e-===SO42-+4H+ |
| D.若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8∶15 |