题目内容
【题目】氮、磷对水体的污染情况越来越受到人们的重视。回答下列问题:
(1)常温下,在pH约为9时,用澄清石灰水可将水体中的HPO42-化为Ca10(PO4)6(OH)2沉淀除去,该反应的离子方程式为_____________。
(2)除去地下水中的硝态氮通常用还原剂将其还原为N2。
①Prusse等提出的用Pd-Cu作催化剂,常温下,在pH为4.0~6.0时,可直接用H2将NO3-还原为N2,该反应的离子方程式为__________。研究发现用H2和CO2的混合气体代替H2,NO3-的去除效果比只用H2时更好,其原因是________。
②在pH约为5时,用纳米Fe粉可将NO3-还原为N2,Fe粉被氧化为Fe2+,该反应中氧化产物与还原产物的物质的量之比为_________。
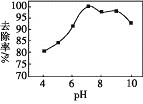
(3)实验测得相同条件下,用次氯酸钠脱除水体中的氨态氮的过程中(2NH3+3ClO-=N2+3H2O+3Cl-),pH与氨态氮的去除率关系如图所示,在pH大于9时,pH越大,去除率越小,其原因是_________。
【答案】10Ca2++8OH-+6HPO42-=Ca10(PO4)6(OH)2↓+6H2O 2NO3-+5H2+2H+![]() N2+6H2O CO2溶于水后呈酸性,可以提供H+,有利于pH维持在4.0~6.0 5∶1 pH大于9时,ClO-的氧化性减弱,不利于氧化NH3
N2+6H2O CO2溶于水后呈酸性,可以提供H+,有利于pH维持在4.0~6.0 5∶1 pH大于9时,ClO-的氧化性减弱,不利于氧化NH3
【解析】
(1)Ca(OH)2与HPO42-反应产生Ca10(PO4)6(OH)2沉淀和水;
(2)①在pH为4.0~6.0的酸性条件下,H2将NO3-还原为N2,CO2溶于水会电离产生H+,便于H2还原NO3-;
②在pH约为5时,纳米Fe粉可将NO3-还原为N2,Fe粉被氧化为Fe2+,根据电子守恒配平方程式,可得该反应中氧化产物与还原产物的物质的量之比;
(3)根据ClO-氧化性与溶液的pH关系分析。
(1)Ca(OH)2与HPO42-反应产生Ca10(PO4)6(OH)2沉淀和水,根据电荷守恒、原子守恒,可得该反应的离子方程式为10Ca2++8OH-+6HPO42-=Ca10(PO4)6(OH)2↓+6H2O;
(2)①在pH为4.0~6.0的酸性条件下,具有还原性的H2可以将NO3-还原为N2,反应的离子方程式为:2NO3-+5H2+2H+![]() N2+6H2O ;若H2中混有CO2,CO2溶于水反应产生的H2CO3发生电离作用,会电离产生H+,有利于pH维持在4.0~6.0,便于H2还原NO3-;
N2+6H2O ;若H2中混有CO2,CO2溶于水反应产生的H2CO3发生电离作用,会电离产生H+,有利于pH维持在4.0~6.0,便于H2还原NO3-;
②在pH约为5时,用纳米Fe粉可将NO3-还原为N2,Fe粉被氧化为Fe2+,根据电子守恒、原子守恒和电荷守恒,可得该反应的化学方程式为:5Fe+12H++2NO3-=5Fe2++N2↑+6H2O,根据方程式可知:在该反应中氧化产物Fe2+与还原产物N2的物质的量之比为5:1;
(3)ClO-具有强的氧化性,溶液的pH越小,ClO-氧化性越强,pH越大,ClO-的氧化性越弱。当pH大于9时,溶液进行较强,则ClO-的氧化性减弱,不利于氧化NH3。