题目内容
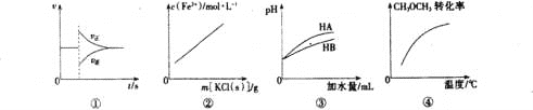
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是( )

A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2的导电能力之和大于HA的
C.b点的混合溶液pH大于7
D.c点的混合溶液中,c(Na+)>c(OH)>c(K+)
【答案】D
【解析】
邻苯二甲酸氢钾为二元弱酸式盐,溶液呈酸性,向邻苯二甲酸氢钾溶液中加入NaOH溶液,二者发生反应生成邻苯二甲酸钾和邻苯二甲酸钠,溶液中离子浓度增加,导电性增强,邻苯二甲酸钾和邻苯二甲酸钠为强碱弱酸盐,邻苯二甲酸根在溶液中水解呈碱性。
A.向邻苯二甲酸氢钾溶液中加入氢氧化钠,二者发生反应生成邻苯二甲酸钾和邻苯二甲酸钠,溶液中的Na+和A2-的浓度增加。由图像可知,溶液导电性增强,说明导电能力与离子浓度和种类有关,A正确;
B.a点和b点K+的物质的量形同,K+的物质的量浓度变化不明显,HA-转化为A2-,b点的导电性强于a点,说明Na+与A2的导电能力之和强于HA-,B正确;
C.b点邻苯二甲酸氢钾溶液与氢氧化钠溶液恰好完全反应生成邻苯二甲酸钾和邻苯二甲酸钠,邻苯二甲酸钾为强碱弱酸盐,A2-在溶液中水解使溶液呈碱性,,溶液pH>7,C正确;
D.b点后继续滴加氢氧化钠溶液,则n(Na+)>n(K+),加入的氢氧根离子在b点之前均参与反应,因此n(Na+)>n(K+)>n(OH),同一体系中体积相同,所以c(Na+)>c(K+)>c(OH),D错误;
故选D。

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
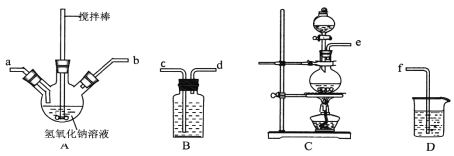
轻松课堂标准练系列答案【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验仪器,用图中的实验装置进行实验,证明过氧化钠可作供氧剂。

(1)A 是制取 CO2 的装置,可选用的试剂_____(填序号)
①碳酸钙固体与稀硫酸 ②碳酸钠固体与稀盐酸 ③碳酸氢钠固体与氢氧化钠溶液
写出对应的离子方程式_________________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和 NaHCO3 溶液 | ____________ |
C | ____________ | 与 CO2 和水反应产生 O2 |
D | NaOH 溶液 | ____________ |
(3)写出过氧化钠与二氧化碳反应的化学方程式_____。
(4)用_____检验 F 中收集到的气体,现象是_____。
【题目】表是25℃时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是
化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
Ksp或Ka | 1.8×10-10 | 2.0×10-12 | 1.8×10-5 | 3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.碳酸钠溶液中滴加少量氯水的离子方程式H2O+CO32-+Cl2=HCO3-+Cl-+HClO
C.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COO-):c(CH3COOH)=9:5,此时溶液pH=5
D.向浓度均为1×10-3mol·L-1的KCl和K2CrO4混合液中滴加1×10-3mol·L-1的AgNO3,CrO42-先沉淀