��Ŀ����
����Ŀ��ij��ѧ��ȤС��������ͼװ��̽����֤��ͭ����Ҫ�ɷ�CuFeS2���ڿ����е��������ﲢ�ⶨCuFeS2�Ĵ��ȣ�����ΪSiO2����
ʵ�鲽�裺����װ�����������װ�õ����������á��ڼ���ҩƷ�����ɼУ�����ڲ��Ϲ���������۵�ȼB���ľƾ���ƣ���������ʯӢ���л�ͭ�����Ʒ��

��ش��������⡣
��1������A�е��Լ���________��������Ϊ________��
��2��Ϊ��������������ͭ����������壬��C��D�е��Լ���ѡ��________����ѡ����
a��Na2S��Һ��NaOH��Һ
b��BaCl2��Һ��NaOH��Һ
c��Ʒ����Һ��NaOH��Һ
d��KMnO4��Һ��NaOH��Һ
��3���������ϣ�
����Ʒ�����պ�õ��Ĺ������Ϊ��ͭ��Cu��Cu2O����������Fe2O3��FeO����
��Cu2O��ϡH2SO4�ķ�ӦΪ��Cu2O��H2SO4��Cu��CuSO4��H2O
̽����Ϊ��֤�����ijɷ֣�ȡ������������������Թ��У�����������ϡ�����ܽ⣬ȡ��������Һ������±��к����ϵ����ݡ�
���� | �����Լ������� | ʵ������ | �ó����� |
��һ�� | ���뼸��K3Fe��CN��6]��Һ | ________ | ��FeO |
�ڶ��� | ���뼸��________��Һ | ��Һ��ΪѪ��ɫ | ��Fe2O3 |
̽�������ʵ�鷽����֤��ͭ���Ƿ���Cu2O��________��
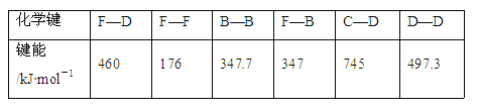
��4��Ϊ�ⶨCuFeS2�Ĵ��ȣ���ȡa g�Ļ�ͭ����Ʒ���ȼ�պס�������ͬѧ�������������ͬ��ʵ�鷽�������´��Ƚ�����ú���Ӧ��ĸ�Ĵ���ʽ��ʾ����
��������C�Թ���Ϊ������H2O2��NaOH�Ļ����Һ���������������C�м��������BaCl2��Һ���Ҿ��ã������˺����õ�����Ϊw g����CuFeS2�Ĵ���Ϊ________��д��C�Թ�����������ʱ���ܷ�Ӧ�����ӷ���ʽ________��
�ҷ��������������ղ����з������ͭ��ʹ����ȫ����ϡ���Ტ���250mL����Һ��ȡ��25.00mL����Һ��c mol��L��1�ı�ҺEDTA����H2Y2����ʾ���ζ����յ㣨�ζ����������ʷ�Ӧ��������EDTA��ҺV mL����CuFeS2�Ĵ���Ϊ________�����ζ�ʱ�ķ�ӦΪ��Cu2����H2Y2����CuY2����2H����
���𰸡���ʯ�� ����ͨ������е�CO2��ˮ���� acd ̽������ɫ���� KSCN�������軯�أ� ̽����ȡ������ͭ���Թ��м�������ϡ���ᣬ����Һ����ɫ˵����ͭ�к���Cu2O�������� ![]() �� SO2 + H2O2 +2OH��= SO42��+ 2H2O
�� SO2 + H2O2 +2OH��= SO42��+ 2H2O ![]() ��
��
��������
����ʵ��ԭ����ʵ��װ�÷���ʵ��װ�õ����ü������Լ�����ɣ��������ӵ����ʷ������ʼ���ķ��������ݵζ�ԭ�������ʼ��ת�����㴿�ȡ�
��1������A�е��Լ��Ǽ�ʯ�ң�������Ϊ����ͨ������еĶ�����̼���ʴ�Ϊ����ʯ�ң�����ͨ������е�CO2��ˮ������
��2������������ͭ�����������Ϊ�����������ö��������Ư���Կ���ʹƷ����ɫ�����ö�������ԭ�ԣ�����ʹ���������Һ��ɫ�����ö������������Կ��Ժ�������Һ��Ӧ���ɻ�ɫ����S�����Ҫ������������Һ����β���������ʴ�Ϊ��acd��
��3��̽����Fe2O3��FeO�ֱ������ᷴӦ������������������������������������K3Fe��CN��6]��Һ��������ɫ������������������KSCN��
̽������Cu2O�ķ�����ȡ������ͭ���Թ��м�������ϡ���ᣬ����Һ����ɫ˵����ͭ�к���Cu2O�������У�
�ʴ�Ϊ����ɫ������KSCN�������軯�أ�ȡ������ͭ���Թ��м�������ϡ���ᣬ����Һ����ɫ˵����ͭ�к���Cu2O�������У�
��4����CuFeS2~2SO2~2BaSO4��
184 233��2
m w
m(CuFeS2)=92w/233
��CuFeS2�Ĵ���Ϊ![]() ����
����
C�Թ���˫��ˮ��ǿ�����ԣ����������½��������������õ����������Ӧ�����ӷ���ʽΪ��SO2 + H2O2 +2OH��= SO42��+ 2H2O��
��CuFeS2~Cu2��~H2Y2���ã�n(CuFeS2)=n(H2Y2��)=c��V��10-2����CuFeS2�Ĵ���Ϊ ![]() �����ʴ�Ϊ��
�����ʴ�Ϊ�� ![]() ����SO2 + H2O2 +2OH��= SO42��+ 2H2O ��
����SO2 + H2O2 +2OH��= SO42��+ 2H2O �� ![]() ����
����

����Ŀ��̼�͵��Ļ����������������й㷺���ڡ��ش���������:
��1�����Ȼ�����NCl3����һ�ֻ�ɫ����״�����д̼�����ζ�Ļӷ����ж�Һ�壬��ԭ�Ӿ�����8e���ṹ��д�������ʽ_____________________���ȼҵ����ʱ������ʳ��ˮ��ͨ����������NH4Cl�����������������ɵ�������Ӧ�����������Ȼ������÷�Ӧ�Ļ�ѧ����ʽΪ______________��
��2����֪��2CO2(g) + 3NaOH(aq)=NaHCO3(aq)+Na2CO3(aq)+H2O(l) ��H=��4a kJ/mol
CO2(g) +2NaOH(aq)=Na2CO3(aq)+H2O(l) ��H=��b kJ/mol
��������CO2��NaOH��Һ��Ӧ����NaHCO3���Ȼ�ѧ��Ӧ����ʽΪ:____________��
��3������CO���Խ�NOת��Ϊ����N2���䷴ӦΪ��2NO(g)+2CO(g)![]() N2(g)+2CO2(g)�����ݻ���ΪIL�ļס��ҡ����������£���Ӧ�¶ȷֱ�Ϊ300�桢T�桢300�棩�����зֱ������ͬ��NO��CO����ø�������n(CO)�淴Ӧʱ��t�ı仯������±���ʾ:
N2(g)+2CO2(g)�����ݻ���ΪIL�ļס��ҡ����������£���Ӧ�¶ȷֱ�Ϊ300�桢T�桢300�棩�����зֱ������ͬ��NO��CO����ø�������n(CO)�淴Ӧʱ��t�ı仯������±���ʾ:
t/min | 0 | 40 | 80 | 120 | 160 |
n(CO)����������/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(CO)����������/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
n(CO)����������/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
�ټ������У�0��40min����NO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(NO)=_______��
�ڸ÷�Ӧ�ġ�H______0���>����<������
�ۼס��������ﵽƽ��ʱ��CO��ת����Ϊ��(��)________��(��)���>��,��< ������������
��4�������£���(NH4)2C2O4��Һ�У���ӦNH4++C2O42��+H2O![]() NH3��H2O+HC2O4����ƽ�ⳣ��K=___������֪�����£�H2C2O4�ĵ���ƽ�ⳣ��Ka1��5��10-2��Ka2��5��10-5 H2O�ĵ���ƽ�ⳣ��Kw=1��10-14 NH3��H2O�ĵ���ƽ�ⳣ��Kb��2��10-5��
NH3��H2O+HC2O4����ƽ�ⳣ��K=___������֪�����£�H2C2O4�ĵ���ƽ�ⳣ��Ka1��5��10-2��Ka2��5��10-5 H2O�ĵ���ƽ�ⳣ��Kw=1��10-14 NH3��H2O�ĵ���ƽ�ⳣ��Kb��2��10-5��
����Ŀ�������ֶ�����Ԫ�أ����ǵĽṹ�����ʵ���Ϣ���±�������
Ԫ�� | �ṹ�����ʵ���Ϣ |
A | �Ƕ�������(��ϡ��������)ԭ�Ӱ뾶����Ԫ�أ���Ԫ�ص�ij�ֺϽ���ԭ�ӷ�Ӧ�ѵĵ��ȼ� |
B | B��Aͬ���ڣ�������������ˮ��������� |
C | Ԫ�ص���̬�⻯�K������ˮ������������� |
D | �Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���Ҳ������ˮ���������г��õ�����ɱ���� |
����ݱ�����Ϣ��д��
��1��Aԭ�ӵĺ�������Ų�ʽ��____________________________________________________��
��2��BԪ�������ڱ��е�λ�ã�________________________________________________�����Ӱ뾶��B________(����ڡ���С�ڡ�)A��
��3��Cԭ�ӵĵ����Ų�ͼ��__________________����ԭ�Ӻ�����________��δ�ɶԵ��ӣ�������ߵĵ���Ϊ________����ϵĵ��ӣ�������________�Ρ�
��4��D���Ľṹʾ��ͼ��________��
��5��B������������Ӧ��ˮ������A������������Ӧ��ˮ���ﷴӦ�Ļ�ѧ����ʽΪ________________________________________________________________________����D���⻯���ˮ���ﷴӦ�Ļ�ѧ����ʽΪ____________________________________________��