题目内容
【题目】已知苯甲酸的酸性比碳酸强,苯酚的酸性比碳酸弱.可以将 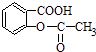 转变为
转变为 ![]() 的方法是( ) ①与足量的NaOH溶液共热,再通入CO2
的方法是( ) ①与足量的NaOH溶液共热,再通入CO2
②与稀硫酸共热后,加入足量的NaOH溶液
③加热溶液,通入足量的SO2
④与稀H2SO4共热后,加入足量的NaHCO3 .
A.①②
B.①④
C.②③
D.②④
【答案】B
【解析】解:①与足量的NaOH溶液共热,羧基与NaOH反应,酯基水解生成苯酚结构与NaOH反应生成苯酚钠,再通入CO2,与苯酚钠结构反应生成产物,故①正确;
②与稀硫酸共热后,加入足量的NaOH溶液,苯酚结构能与NaOH反应,则不能得到产物,故②错误;
③加热溶液,通入足量的SO2,不能得到羧酸钠结构,故③错误;
④与稀H2SO4共热后,酯基水解生成苯酚结构,加入足量的NaHCO3,羧基与NaHCO3反应得到产物,故④正确;
故选B.

练习册系列答案
相关题目
【题目】下列选用的仪器和药品能达到实验目的是( )
A | B | C | D |
|
| 饱和NaHSO3溶液 | |
制乙炔的发生装置 | 蒸馏时的接收装置 | 除去SO2中的少量HCl | 准确量取一定体积K2Cr2O7标准溶液 |
A.A
B.B
C.C
D.D




