题目内容
【题目】采用乙烯与甲苯为主要原料,按下列路线可合成有机物 E、F:
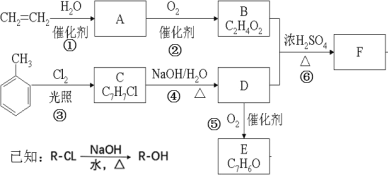
请回答:
(1)B 中官能团的名称是_________,反应⑥的反应类型是__________。
(2)D→E 的 化 学 方 程 式_________________________________。
(3)F 的 结 构 简 式___________________________。
(4)下列有关说法不正确的是_________。
A.E 能与新制的 Cu(OH)2 悬浊液发生反应,而 B 不能与新制的 Cu(OH)2 悬浊液发生反应
B.F 在碱性条件下可发生皂化反应
C. ![]() 不能使酸性 KMnO4 溶液褪色
不能使酸性 KMnO4 溶液褪色
D. 1mol E 和足量 H2 反应,最多消耗 4mol H2
【答案】羧基 取代(酯化)反应 ![]()
![]() A、B、C
A、B、C
【解析】
由转化关系图可知,乙烯和水反应生成A为乙醇。乙醇催化氧化最终生成B乙酸,甲苯和氯气在光照条件下甲基上的氢原子被取代生成C为![]() ,
,![]() 在碱性条件下发生水解生成D为苯甲醇,苯甲醇和乙酸发生酯化反应生成F为乙酸苯甲酯,苯甲醇催化氧化生成苯甲醛。
在碱性条件下发生水解生成D为苯甲醇,苯甲醇和乙酸发生酯化反应生成F为乙酸苯甲酯,苯甲醇催化氧化生成苯甲醛。
(1)由以上分析可知B是乙酸,所含官能团为羧基,反应⑥是乙酸和苯甲醇的酯化反应;
本题答案为:羧基、取代反应(酯化反应)。
(2)D是苯甲醇,E是苯甲醛,D→E 的 化 学 方 程 式为:![]() ;
;
本题答案为:![]() 。
。
(3)F是乙酸苯甲酯,结构简式为: ![]() ;
;
本题答案为:![]() 。
。
(4)A. E 是苯甲醛,能与新制的 Cu(OH)2 悬浊液发生反应,而 B是乙酸也能与新制的 Cu(OH)2 悬浊液发生反应,故A错误;
B. 通常油脂在强碱溶液中的反应称为皂化反应,F 是乙酸苯甲酯,在碱性条件下可发生水解反应,但不是皂化反应,故B错误;
C. ![]() 能被酸性高锰酸钾氧化成苯甲酸,所以能使酸性 KMnO4 溶液褪色,故C错误;
能被酸性高锰酸钾氧化成苯甲酸,所以能使酸性 KMnO4 溶液褪色,故C错误;
D.E是苯甲醛,苯环和醛基均能和H2发生加成反应,1mol E 和足量 H2 反应,最多消耗 4mol H2,故D正确;
本题答案为:ABC。