��Ŀ����
����Ŀ��Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ġ���֪��ˮ��ȡþ����Ҫ�������£�

(1)���ڼ����Լ������������������¼��ֲ�ͬ������������������⡣
���� | �Ƿ���ȷ | �������� |
����1��ֱ������ˮ�м�������� | ����ȷ | (һ) |
����2�����¼���������ˮ���ټ�������� | (��) | (��) |
����Ϊ����������������ǣ�����������(��) | ||
(һ)__________________________________________________��
(��)__________________________________________________��
(��)__________________________________________________��
(��)__________________________________________________��
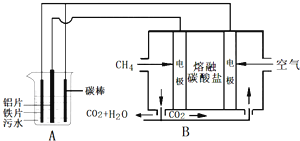
(2)��ͼ�м�����Լ���Ӧ����________(�ѧʽ)��������Լ�����________(�ѧʽ)����ҵ������ˮMgCl2��ȡþ�Ļ�ѧ����ʽΪ___________��
���𰸡� ��ˮ��þ����Ũ��С������������������ ����ȷ ��Դ���Ĵ����� ��̲ɹ�κ�õ��Ŀ�±ˮ�У���������� Ca(OH)2 HCl MgCl2(����)![]() Mg��Cl2��
Mg��Cl2��
����������1���Լ���Ӧ��ʯ�����������ķ�Ӧ��MgCl2��Ca(OH)2===Mg(OH)2����CaCl2�����ں�ˮ��þ����Ũ��С������������������������ֱ������ˮ�м���������Ǵ���ģ����¼���������ˮ��Դ���Ĵ����������Ҳ�Ǵ���ģ���2��������þ�����ᷴӦ�õ��Ȼ�þ�������Լ���Ӧ����������Ӧ��Mg(OH)2��2HCl===MgCl2��2H2O��Ȼ��Ũ�����ᾧ����ˮ����ˮMgCl2���ٵ�����ڵ�MgCl2����Ƶ�Mg��MgCl2(����)![]() Mg��Cl2����
Mg��Cl2����