题目内容
15.下列实验操作和现象及其结论正确的是( )| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均变性了 |
| B | 将淀粉溶液和稀H2SO4混合加热后,再滴加新制的Cu(OH)2悬浊液,煮沸 | 无砖红色沉淀产生 | 淀粉未水解 |
| C | 向苯酚浓溶液中滴加少量溴水,振荡 | 无白色沉淀 | 苯酚与溴水不反应 |
| D | CH3COOH、C2H5OH和浓H2SO4共热制备CH3COOC2H5,将共热后产生的气体导入盛有饱和Na2CO3溶液的试管中 | 有油状物浮于Na2CO3溶液表面,振荡后,油状层变薄 | 证明油状物不全部是CH3COOC2H5 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.分别滴加饱和NaCl溶液和CuSO4溶液,分别发生盐析和变性;
B.淀粉溶液和稀H2SO4混合加热后,发生水解,检验葡萄糖应在碱性溶液中;
C.滴加少量溴水,生成的三溴苯酚易溶于苯;
D.碳酸钠溶液可吸收乙醇,与乙酸反应,降低乙酸乙酯的溶解度,反应后分层.
解答 解:A.分别滴加饱和NaCl溶液和CuSO4溶液,分别发生盐析和变性,均有固体析出,结论不合理,故A错误;
B.淀粉溶液和稀H2SO4混合加热后,发生水解,检验葡萄糖应在碱性溶液中,则加碱至碱性再加新制的Cu(OH)2悬浊液,煮沸来检验,操作和现象及其结论均不合理,故B错误;
C.滴加少量溴水,生成的三溴苯酚易溶于苯,则不能观察到白色沉淀,应利用浓溴水,操作和现象及其结论均不合理,故C错误;
D.碳酸钠溶液可吸收乙醇,与乙酸反应,降低乙酸乙酯的溶解度,反应后分层,有油状物浮于Na2CO3溶液表面,振荡后,油状层变薄,可证明油状物不全部是CH3COOC2H5,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的结构与性质、混合物分离提纯等,把握物质的性质、实验技能及实验细节为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
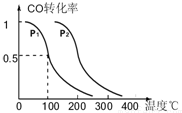
20.已知反应A2(g)+2B2(g)?2AB2(g)的△H<0,下列说法正确的是( )
| A. | 升高温度,A2转化率增大 | |
| B. | 升高温度有利于速率增大,从而缩短达到平衡的时间 | |
| C. | 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 | |
| D. | 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
6.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如图所示:

(1)酸溶过程中为提高铁的浸出率,可采取的措施有适当提高反应温度(增加浸出时间;增大硫酸的浓度;研磨硫酸渣,增大固体表面积)(要求写出一条).“滤渣A”主要成份的化学式为SiO2.
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2+14Fe3++8H2O═15Fe2++2SO42-.
(3)氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
(4)为了确保铁红的质量,氧化过程需要调节溶液的pH的范围是3.2-3.8(几种离子沉淀的pH见表);滤液B可以回收的物质有(写化学式)Na2SO4、Al2(SO4)3、MgSO4,.

(1)酸溶过程中为提高铁的浸出率,可采取的措施有适当提高反应温度(增加浸出时间;增大硫酸的浓度;研磨硫酸渣,增大固体表面积)(要求写出一条).“滤渣A”主要成份的化学式为SiO2.
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2+14Fe3++8H2O═15Fe2++2SO42-.
(3)氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
3.下列物质属于天然高分子的是( )
| A. | 蛋白质 | B. | 天然气 | C. | 聚乙烯 | D. | 葡萄糖 |
10.下列物质中能发生消去反应的是( )
| A. | (CH3)3CCH2Br | B. | CH3Br | C. | 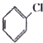 | D. |  |
20.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色粘稠液体,易溶于水.为研究A的组成和结构,进行如下实验:
已知:①2R-COOH+2Na→2R-COONa+H2↑
②R-COOH+NaHCO3→R-COONa+CO2↑+H2O
已知:①2R-COOH+2Na→2R-COONa+H2↑
②R-COOH+NaHCO3→R-COONa+CO2↑+H2O
| 实验步骤 | 解释或实验结论 |
| (1)取9.0g有机物A加热使其气化,测得其密度是相同条件下H2的45倍 | (1)由此可知A的相对分子质量为90. |
| (2)将9.0gA在足量O2中充分燃烧,其产物依次缓缓通过浓硫酸、碱石灰,两者分别增重5.4g和13.2g. | (2)由此可知A的分子式为C3H6O3. |
| (3)另取A9.0g,跟足量的NaHCO3粉末反应,生成CO2气体2.24L;9.0gA若与足量金属钠反应生成H2也是2.24L(气体体积皆为标准状况下测得). | (3)由此可知A中含有官能团有.(填结构简式)-COOH、-OH |
(4)A的核磁共振氢谱如下图: | (4)由此可知A中含有4种不同性质的氢原子 (5)综上,A的结构简式为  . . |
7.氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图,下列有关氢氧燃料电池的说法不正确的是( )
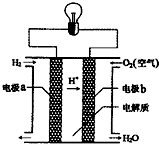

| A. | a电极是负极 | |
| B. | 该电池的总反应:2H2+O2═2H2O | |
| C. | 产物为无污染的水,属于环境友好电池 | |
| D. | 外电路中电子b电极通过导线流向a电极 |
5.下列物质中,不能发生消去反应的是( )
| A. | 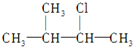 | B. | CH2BrCH2Br | ||
| C. | 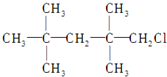 | D. | CH2ClCH2CH3 |