题目内容
【题目】将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐(pH=2.5)中的葡萄糖转化成葡萄糖内酯并获得能量。下列说法正确的是
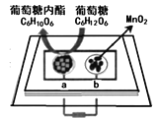
A.a极为正极
B.外电路电子移动方向为b到a
C.b极的电极反应式为:MnO2+2H2O+2e-=Mn2++4OH-
D.当消耗0.01mol葡萄糖时,电路中转移0.02mol电子
【答案】D
【解析】
A.根据图知:葡萄糖C6H12O6转化为葡萄糖内酯C6H10O6,C元素化合价由0价转化为+![]() ,则该电极上失电子发生氧化反应,所以a为负极,b为正极,故A错误;
,则该电极上失电子发生氧化反应,所以a为负极,b为正极,故A错误;
B. 外电路电子移动方向为由负极a到正极b,故B错误;
C.b电极上二氧化锰得电子和氢离子反应生成水和锰离子,电极反应式为MnO2+4H++2e-=Mn2++2H2O ,故C错误;
D.根据C6H12O6- 2e-= C6H10O6 + 2H +知,消耗1mol葡萄糖转移2mol电子,则消耗0.01mol葡萄糖转移0.02mol电子,故D正确;
故答案:D。

 名校课堂系列答案
名校课堂系列答案【题目】已知:①1mol晶体硅中含有2molSi—Si键。
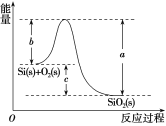
②Si(s)+O2(g)===SiO2(g) ΔH,其反应过程与能量变化如图所示。
③
化学键 | Si—O | O=O | Si—Si |
断开1 mol共价键所需能量/kJ | 460 | 500 | 176 |
下列说法中正确的是( )
A.晶体硅光伏发电是将化学能转化为电能B.二氧化硅稳定性小于硅的稳定性
C.ΔH=-988kJ·mol-1D.ΔH=(a-c)kJ·mol-1
【题目】探究2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O反应速率的影响因素,有关实验数据如下表所示:
实验 编号 | 温度 (℃) | 催化剂用量(g) | 酸性KMnO4溶液 | H2C2O4溶液 | KMnO4 溶液褪色平均时间(min) | ||
体积 (mL) | 浓度 (mol·L-1) | 体积 (mL) | 浓度 (mol·L-1) | ||||
1 | 25 | 0.5 | 4 | 0.1 | 8 | 0.2 | 12.7 |
2 | 80 | 0.5 | 4 | 0.1 | 8 | 0.2 | a |
3 | 25 | 0.5 | 4 | 0.01 | 8 | 0.2 | 6.7 |
4 | 25 | 0 | 4 | 0.01 | 8 | 0.2 | b |
下列说法不正确的是
A.反应速率:v(实验3) > v(实验1)
B.a<12.7,b>6.7
C.用H2C2O4表示实验1的反应速率:v(H2C2O4)≈6.6×l0-3mol·L-1·min-1
D.相同条件下可通过比较收集相同体积CO2所消耗的时间来判断反应速率快慢