题目内容
【题目】乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得。
I.制备碳酸亚铁:装置如图所示。
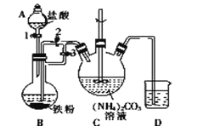
(1)B中可观察到的现象是铁粉逐渐溶解,_________________________。
将B中生成的FeCl2溶液压入装置C的操作是______________________。
Ⅱ.制备乳酸亚铁:
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。
(2)加入少量铁粉的作用是___________________,反应后加入适量乳酸的作用是________________。
(3)从所得溶液中获得乳酸亚铁晶体所需的实验操作是______ _、______、洗涤、干燥。
(4)设计实验证明乳酸亚铁中含Fe2+ ____________________ _。
【答案】(1)有气泡冒出,溶液变成浅绿色;关闭活塞3,打开活塞2(各2分)
(2)防止Fe2+被氧化;除去铁粉(各1分)
(3)冷却结晶;过滤(各1分)
(4)取少量乳酸亚铁溶液于试管中,先滴加几滴KSCN溶液,溶液不变色,再滴加新制氯水,溶液变成血红色(或其他合理答案)(2分)
【解析】
试题分析:(1)Fe与稀盐酸会发生反应:Fe+2HCl=FeCl2+H2↑,因此会观察到有气泡冒出,溶液变成浅绿色;将B中生成的FeCl2溶液压入装置C的操作是关闭活塞3,打开活塞2,在氢气压强的作用下,FeCl2溶液被压入装置C;(2)Fe2+具有还原性,容易被装置中的空气氧化产生Fe3+,为防止其变质,要加入还原铁粉;Fe是比较活泼的金属,可以与酸发生反应,所以反应后加入适量乳酸的作用是除去过量的铁粉;(3)乳酸亚铁的溶解度受温度的影响变化较大,从所得溶液中获得乳酸亚铁晶体所需的实验操作是蒸发浓缩、冷却结晶、过滤、洗涤、干燥;(4)证明乳酸亚铁中含Fe2+的实验是取少量乳酸亚铁溶液于试管中,先滴加几滴KSCN溶液,溶液不变色,再滴加新制氯水,溶液变成血红色。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】化学在生活中有着广泛的应用,下列对应关系错误的是
化学性质 | 实际应用 | |
A | 乙酸具有酸性 | 常用于除水垢 |
B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
C | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
D | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |