题目内容
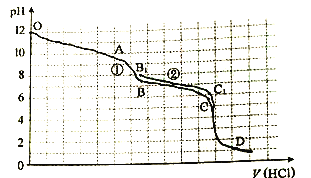
【题目】25℃时,向Na2CO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。
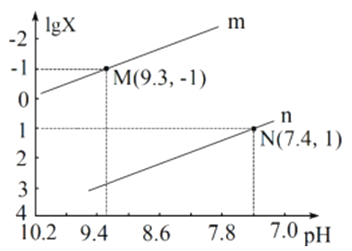
已知:lgX=lg![]() 或lg
或lg![]() ,下列叙述正确的是
,下列叙述正确的是
A. 曲线m表示pH与lg![]() 的变化关系
的变化关系
B. 当溶液呈中性时,c(Na+)=![]() +2
+2![]()
C. Ka1(H2CO3)=1.0×10-6.4
D. 25℃时,CO32-+H2O![]()
![]() +OH-的平衡常数为1.0×10-7.6
+OH-的平衡常数为1.0×10-7.6
【答案】C
【解析】
A、碳酸钠溶液中滴加盐酸,发生反应CO32-+H+![]() HCO3-、HCO3-+H+
HCO3-、HCO3-+H+![]() H2O+CO2↑,根据图像,推出曲线m表示的是
H2O+CO2↑,根据图像,推出曲线m表示的是![]() ,选项A错误;B、根据电中性,c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),因为溶液显中性,因此c(H+)=c(OH-),即得出c(Na+)=c(HCO3-)+2c(CO32-),选项B错误;C、n曲线代表的是
,选项A错误;B、根据电中性,c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),因为溶液显中性,因此c(H+)=c(OH-),即得出c(Na+)=c(HCO3-)+2c(CO32-),选项B错误;C、n曲线代表的是![]() ,N点,c(HCO3-) c(H2CO3)=10,此时c(H+)=10-7.4mol/L,根据电离平衡常数的定义,H2CO3的一级电离平衡常数为
,N点,c(HCO3-) c(H2CO3)=10,此时c(H+)=10-7.4mol/L,根据电离平衡常数的定义,H2CO3的一级电离平衡常数为![]() ,选项C正确;D、该反应的平衡常数为
,选项C正确;D、该反应的平衡常数为![]() ,根据M点,c(HCO3-) c(H2CO3)=10,c(H+)=10-9.3mol/L,c(OH-)=10-4.7mol/L,代入数值,得出此反应的化学平衡常数为10-3.7,选项D错误。答案选C。
,根据M点,c(HCO3-) c(H2CO3)=10,c(H+)=10-9.3mol/L,c(OH-)=10-4.7mol/L,代入数值,得出此反应的化学平衡常数为10-3.7,选项D错误。答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目