题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA
B.14g分子式为CnH2n的链烃中含有的C-H键的数目为2NA
C.室温时,1.0 L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA
D.Fe与水蒸气反应生成22.4L氢气,转移电子数为2NA
【答案】B
【解析】
试题分析:A、标准状况下乙醇是液体,不能利用气体摩尔体积计算分子数,A错误;B、14g分子式为CnH2n的链烃中含有的C-H键的物质的量是![]() ,数目为2NA,B正确;C、室温时,1.0 L pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA,C错误;D、Fe与水蒸气反应生成22.4L氢气,应用不能确定氢气是否处于标准状况下,则不能计算转移电子数,D错误,答案选B。
,数目为2NA,B正确;C、室温时,1.0 L pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA,C错误;D、Fe与水蒸气反应生成22.4L氢气,应用不能确定氢气是否处于标准状况下,则不能计算转移电子数,D错误,答案选B。

 阅读快车系列答案
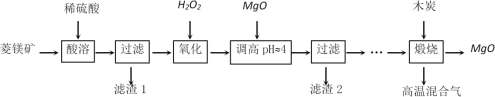
阅读快车系列答案【题目】用软锰矿[主要成分MnO2,还含SiO2 、Fe2O3、Al2O3、Cu2(OH)2CO3的等杂质]和酸洗厂废酸液(含1mol/LH2SO4的FeSO4溶液)联合生产硫酸锰和铁红(Fe2O3)生产过程如下

Mn(OH)2 | Fe(OH)2 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | |
开始沉淀时 | 8.3 | 6.3 | 4.7 | 3.4 | 2.7 |
完全沉淀时 | 9.8 | 8.3 | 6.7 | 4.4 | 3.2 |
(1)含杂质的软锰矿使用前需将其粉碎,目的是______。
(2)滤渣1中含有的主要物质是_______。
(3)滤液1中,加氨水调控溶液pH至3.2,通入O2,反应的离子方程式是_______。若用H2O2代替O2,是否合理?理由是___________。
(4)软锰矿粉与硫酸和硫酸亚铁溶液反应的离子方程式是_________。
(5)滤液3中加入难溶电解质MnS的目的是(用离子方程式表示)_________。
(6)用重结晶法从滤液4中获取硫酸锰晶体的操作是:__________。