题目内容
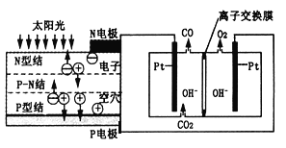
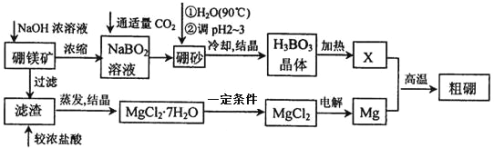
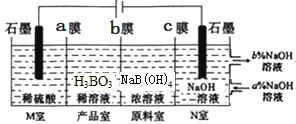
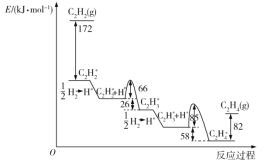
【题目】如下图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。
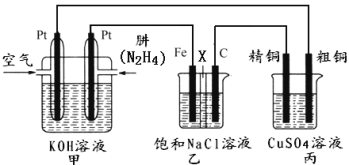
根据要求回答相关问题:
(1)甲装置中通入____气体的一极为正极,其电极反应式为:__________。
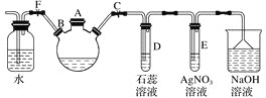
(2)乙装置中石墨电极为_____极(填“阳”或“阴”,其电极反应式为_____;可以用_____检验该反应产物,电解一段时间后,乙池中的溶液呈_________性。
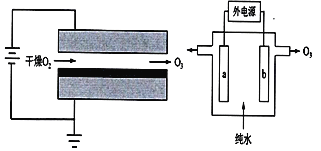
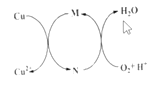
(3)图中用丙装置模拟工业中的_________原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为_________g。
(4)如果将丙中的粗铜电极换为Pt电极,则丙中总化学方程式为________。
【答案】空气 O2+4e-+2H2O=4OH- 阳 2Cl--2e-=Cl2↑ 湿润的淀粉碘化钾试纸 碱 粗铜的精炼 0.8 2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4
2Cu+O2↑+2H2SO4
【解析】
(1)根据原电池反应原理,负极上失电子,正极上得电子,则正极上氧气得电子发生还原反应,电极反应式为:O2+4e-+2H2O=4OH-;答案为空气,O2+4e-+2H2O=4OH-。
(2)乙装置中石墨与电源正极相接,为阳极,阳极上氯离子失去电子生成氯气,发生氧化反应,电极反应式为2Cl--2e-=Cl2↑,检验氯气的方法是用湿润的淀粉碘化钾试纸,观察是否变蓝,电解食盐水的总反应为2H2O+2Cl-![]() Cl2↑+H2↑+2OH-,电解后的溶液呈碱性;答案为阳,2Cl--2e-=Cl2↑,湿润的淀粉碘化钾试纸,碱。
Cl2↑+H2↑+2OH-,电解后的溶液呈碱性;答案为阳,2Cl--2e-=Cl2↑,湿润的淀粉碘化钾试纸,碱。
(3)装置丙中,粗铜作阳极,纯铜作阴极,所以该装置为粗铜精炼装置;原电池负极和纯铜电极上有:N2H4~N2~4e-,Cu~Cu2+~2e-,根据电子守恒得到关系式:N2H4~2Cu,n(N2H4)=![]() n(Cu)=
n(Cu)= ![]() ×
×![]() =0.025mol,m(N2H4)=nM=0.025mol×32g/mol=0.8g;答案为粗铜的精炼,0.8。
=0.025mol,m(N2H4)=nM=0.025mol×32g/mol=0.8g;答案为粗铜的精炼,0.8。
(4)将丙中的粗铜电极换为Pt电极,则Pt电极为惰性电极,装置为电解硫酸铜溶液装置,溶液中铜离子和氢氧根离子放电,生成Cu和O2,电解硫酸铜溶液的化学方程式为2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4;答案为2CuSO4+2H2O
2Cu+O2↑+2H2SO4;答案为2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4。
2Cu+O2↑+2H2SO4。