题目内容
(1)硫酸铵中氮元素的质量分数是___。
(2)实验测得某硫酸铵肥料氮元素的质量分数为20%,则该样品中可能混有( )。
A.碳酸氢铵 B.硝酸铵 C.氯化铵 D.磷酸氢二铵[( NH4)2HPO4]
(2)A

(11 分)科学家一直致力研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3,反应的化学方程式如下:N2(g)+ 3H2O(l)  2NH3(g)+ O2(g)。回答下列问题:
2NH3(g)+ O2(g)。回答下列问题:
(1)进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压力1.0×105 Pa、反应时间3 h),则该反应的正反应为 反应(填“吸热”或“放热”)
|
T/K |
303 |
313 |
323 |
|
NH3生成量/(10-6 mol) |
4.8 |
5.9 |
6.0 |
(2)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议: 。
(3)合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)。部分物质的燃烧热数
据如下:
H2(g) :△H =-285.8 kJ・mol-1;
CO(g) : △H =-283.0 kJ・mol-1;
CH4(g) :△H =-890.3 kJ・mol-1 。
已知1mol H2O(g)转变为1mol H2O(l)时放出44.0 kJ热量。写出CH4和H2O在高温下反应的热化学方程式__________________________________。
(4)有人设想寻求适合的催化剂和电极材料,以N2、H2为电极反应物,以HCl——NH4Cl为电解质溶液制成新型燃料电池,请写出该电极的正极反应式
(5)生成的NH3可用于制铵态氮肥,如(NH4)2SO4、NH4Cl,这些肥料显 性,原因是(用离子方程式表示)___________________________,使用时避免与________________物质合施。
 NH3H2O+H+
NH3H2O+H+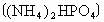
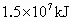 ,已知
,已知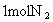 和
和 化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.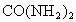 〕.
〕.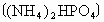
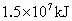 ,已知
,已知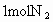 和
和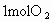 化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.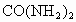 〕.
〕.