题目内容
【题目】把l00mL2.0 mol/L CuSO4溶液和l00 mL l.0 mol/LH2SO4溶液混合(假设混合后溶液的体积等于混合前两种溶液的体积之和)。计算
(1)混合溶液中CuSO4的物质的量浓度。
(2)混合溶液中SO42-的物质的量浓度。
【答案】(1)1mol/L ;(2)1.5mol/L
【解析】
试题分析:根据c=![]() 可得混合前:n(CuSO4)=2.0mol/L×0.1L=0.2mol,n(H2SO4)=l.0mol/L×0.1L=0.1mol,
可得混合前:n(CuSO4)=2.0mol/L×0.1L=0.2mol,n(H2SO4)=l.0mol/L×0.1L=0.1mol,
(1)混合后溶液的体积为0.2L,c(CuSO4)=![]() =1mol/L,
=1mol/L,
故答案为:混合溶液中CuSO4的物质的量浓度为1mol/L;
(2)混合后:n(SO42-)=n(CuSO4)+n(H2SO4)=0.2mol+0.1mol=0.3mol,混合后c(SO42-)=![]() =1.5mol/L;
=1.5mol/L;
故答案为:混合溶液中SO42-的物质的量浓度分别为1.5mol/L。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
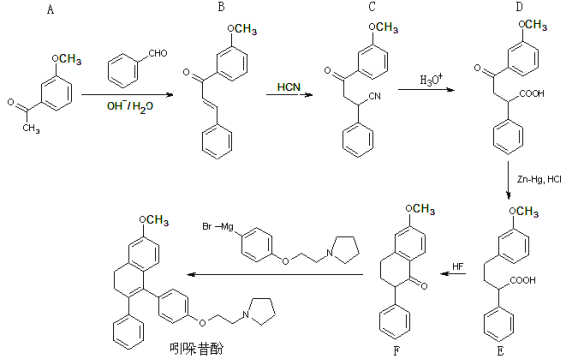
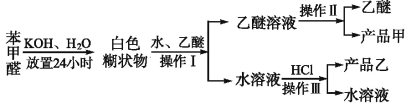
综合自测系列答案【题目】有机合成在制药工业上有着极其重要的地位。现用硝基苯制取苯胺,再用苯胺制得无 色晶体乙酰苯胺(具有退热镇痛作用的药物)。
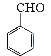
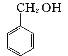
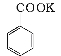
①化学反应原理为:
![]()
②相关物质的物理常数
物质 | 相对分子质量 | 熔点(℃) | 沸点(℃) | 溶解度(g) | |
水 | 乙醇 | ||||
苯胺 | 93 | -6 | 184 | 3.42(20℃) | 任意比混溶 |
乙酸 | 60 | 17 | 117.9 | 任意比混溶 | 任意比混溶 |
乙酰苯胺 | 135 | 114 | 304 | 0.56(20℃) 3.45(50℃) 5.20(100℃) | 36.9(20℃) |
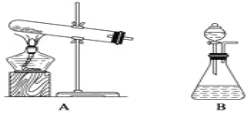
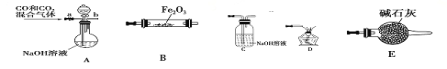
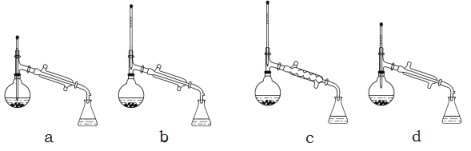
③制备乙酰苯胺的装置及过程如下图所示:
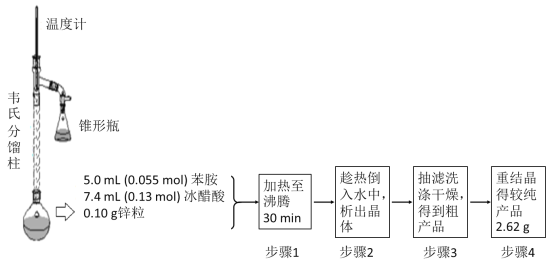
已知:Ⅰ苯胺易被氧化;Ⅱ韦氏分馏柱作用与原理类似于冷凝管
请回答以下问题:
(1)加入锌粒的目的是___________;韦氏分馏柱作用的是_________;
(2)步骤1中保持柱顶温度约为105℃,则锥形瓶中收集到的馏分主要是_____________;
(3)步骤2中将反应液倒入水中的目的是___________;
(4)步骤3中洗涤剂最好选择______________;
A.冷水 B.热水 C.15%的乙醇溶液 D.NaOH溶液
(5)步骤4重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→________→__________→抽滤→洗涤→干燥;
(6)上述制备过程的产率是____________。(结果保留4位有效数字)。