题目内容
7.下列仪器的刻度位置不正确的是( )| A. | 100 mL量筒的0刻度在最下方 | |
| B. | 天平上游码标尺最左方的刻度为0 | |
| C. | 一般温度计的0刻度在中间位置 | |
| D. | 容量瓶的刻度无数字,只是瓶颈上的一个水平环 |
分析 A.量筒没有零刻度;
B.游码标尺有零刻度;
C.温度计能够测量0上和0下温度,0刻度在中间;
D.容量瓶只有一个刻度.
解答 解:A.量筒没有零刻度,故A错误;
B.游码标尺有零刻度,最左方的刻度为0,故B正确;
C.温度计0刻度在温度计的中间部分,故C正确;
D.容量瓶只有一个刻度,是瓶颈上的一个水平环,故D正确.
故选A.
点评 本题考查了计量仪器的构造及使用方法,题目难度不大,注意掌握常见计量仪器的构造,实验中的计量仪器都有一定的刻度,要了解这些刻度的变化情况,如量筒是没有0刻度的,是易错点.

练习册系列答案
相关题目
18.为了探究AgNO3的热稳定性和氧化性,某化学兴趣小组设计了如下实验.
Ⅰ.AgNO3的热稳定性
利用如图所示的实验装置,加热A 中的AgNO3同体,试管A中有红棕色气体产生,B中无红棕色气体产生,在装置C中收集到无色气体.当反应结束后,测得试管中残留黑色同体Ag.(夹持及加热仪器均省略)

(1)如何检验整套装置的气密性?
(2)C中集气瓶收集的气体为氧气,要收集纯净的该气体,正确的操作是等到导气管中气泡均匀放出时再收集.
(3)AgNO3分解的化学方程式为2AgNO3△_△––––––2Ag+2NO2↑+O2↑.
Ⅱ.AgNO3的氧化性
将光亮的铁丝伸入盛有AgNO3 溶液的大试管中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,
猜测如下:
假设一:Fe被氧化成Fe2+;
假设二:Fe被氧化成Fe3+;
假设三:Fe被氧化成Fe2+ 和Fe3+.
已知:溶液中的Ag+能与SCN-反应,干扰实验.选用如下试剂设计一个实验验证假设三.
可选用的试剂:KSCN溶液、酸性 KMnO4溶液、氯水、盐酸、硝酸、NaCl溶液.
请完成下表:
实验结论:Fe的氧化产物为Fe2+ 和Fe3+.
Ⅰ.AgNO3的热稳定性
利用如图所示的实验装置,加热A 中的AgNO3同体,试管A中有红棕色气体产生,B中无红棕色气体产生,在装置C中收集到无色气体.当反应结束后,测得试管中残留黑色同体Ag.(夹持及加热仪器均省略)

(1)如何检验整套装置的气密性?
(2)C中集气瓶收集的气体为氧气,要收集纯净的该气体,正确的操作是等到导气管中气泡均匀放出时再收集.
(3)AgNO3分解的化学方程式为2AgNO3△_△––––––2Ag+2NO2↑+O2↑.
Ⅱ.AgNO3的氧化性
将光亮的铁丝伸入盛有AgNO3 溶液的大试管中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,
猜测如下:
假设一:Fe被氧化成Fe2+;
假设二:Fe被氧化成Fe3+;
假设三:Fe被氧化成Fe2+ 和Fe3+.
已知:溶液中的Ag+能与SCN-反应,干扰实验.选用如下试剂设计一个实验验证假设三.
可选用的试剂:KSCN溶液、酸性 KMnO4溶液、氯水、盐酸、硝酸、NaCl溶液.
请完成下表:
| 操作 | 现象 | 结论或目的 |
| (1)取少量溶液于试管中,向溶液中加入足量NaCl溶液 | - | 除尽Ag+ |
| (2)取少量上述溶液于试管中,加入KSCN溶液,振荡 | 溶液变血红色 | 存在Fe3+ |
| (3)取(1)中少量上述溶液于试管中,加入酸性KMnO4溶液,振荡 | 血红色消失 | 存在Fe2+ |
15.化学家于1995年合成了一种分子式为C200H200的含有多个碳碳叁键的链烃,其分子中含有碳碳叁键数目最多可以是( )
| A. | 49 | B. | 50 | C. | 51 | D. | 无法确定 |
2.a mol Cu与含b mol HNO3的溶液恰好完全反应,则被还原的HNO3的物质的量一定是( )
| A. | (b-2a) mol | B. | b2b2mol | C. | 2a32a3 mol | D. | 2a mol |
12.下列反应中,属于加成反应的是( )
| A. | CH4+Cl2光照→CH3Cl+HCl | B. | CH2═CH2+HCl一定条件→CH3CH2Cl | ||
| C. | 2CH3CH2OH+O2△→2CH3CHO+2H2O | D. |  +BrFeBr3→ +BrFeBr3→ +HBr +HBr |
19.下列除去杂质的方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 二氧化碳 | 一氧化碳 | 点燃 |
| B | 铁粉 | 铜粉 | 过量稀硫酸溶液、过滤 |
| C | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D | 一氧化碳 | 二氧化碳 | 通过足量灼热的氧化铜 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
17.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,18gD2O中所含的电子数为10NA | |
| B. | 200mL0.5mol•L-1的Na2CO3溶液中,由于CO32-水解,所以阴离子数目小于0.1NA | |
| C. | 精炼铜时,当阳极质量减少6.4g时,电路中转移电子数不一定为0.2NA | |
| D. | 5.6g铁与足量稀硫酸反应失去电子数为0.3NA |
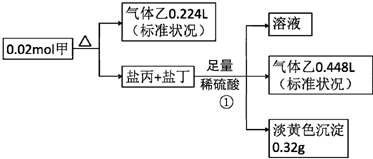
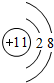 ,甲的化学式Na2S2O4
,甲的化学式Na2S2O4 A~F是初中化学常见的六种物质,它们之间的关系如图所示.“→”表示物质间的转化关系,“--”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成.
A~F是初中化学常见的六种物质,它们之间的关系如图所示.“→”表示物质间的转化关系,“--”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成.