题目内容
【题目】纳米级Fe3O4是一种非常重要的磁性材料,同时也可用作催化剂载体和微波吸收材料。納米级Fe3O4有多种不同制法,请回答下列相关问题。
I.下图是用共沉淀法制备纳米四氧化三铁的流程。
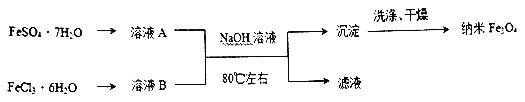
(1)除Fe3O4外铁的两种常见氧化物中在空气中性质比较稳定的是_______(填化学式),该物质的用途是___________(任写一种)。
(2)实验室保存溶液B 时为了防止出现浑浊通常采用的措施是___________ 。
(3)证明沉淀已经洗涤干净的操作是___________ 。
(4)写出该方法中发生的主要反应的离子方程式___________ 。
(5)实际生产中为提高产率,起始所用FeSO4·7H2O 和FeCl3·6H2O 的物质的量之比大于1:2,原因是___________。
II.制备纳米四氧化三铁的另一种流程如下图所示。
![]()
(6)写出第2 步反应的化学方程式______________,其中氧化产物和还原产物的物质的量之比为______。
(7)纳米Fe3O4投入分散剂中形成的分散系是______________。
【答案】 Fe2O3 红色油漆、涂料、炼铁 加盐酸 少量最后一次洗涤液于试管中,加盐酸酸化,滴加氯化钡溶液,不产生白色沉淀 Fe2++2Fe3++8OH-![]() Fe3O4+4H2O 反应过程中部分亚铁离子被氧气氧化为铁离子 6FeOOH+CO=2Fe3O4+CO2+3H2O 1:2 胶体
Fe3O4+4H2O 反应过程中部分亚铁离子被氧气氧化为铁离子 6FeOOH+CO=2Fe3O4+CO2+3H2O 1:2 胶体
【解析】(1)FeO(氧化亚铁) FeO是一种 黑色粉末,不稳定,在空气里受热,就迅速被氧化成 Fe3O4,除Fe3O4外铁的两种常见氧化物中在空气中性质比较稳定的是Fe2O3,Fe2O3用途是红色油漆、涂料、炼铁;(2)实验室保存溶液BFeCl3时为了防止水解出现浑浊,通常采用的措施是加盐酸抑制FeCl3水解生成Fe(OH)3沉淀。(3)证明沉淀已经洗涤干净,只要检验洗涤液中是否含硫酸根离子,操作是少量最后一次洗涤液于试管中,加盐酸酸化,滴加氯化钡溶液,不产生白色沉淀;(4)该方法中发生的主要反应的离子方程式Fe2++2Fe3++8OH-![]() Fe3O4+4H2O ;(5)实际生产中为提高产率,起始所用FeSO4·7H2O和FeCl3·6H2O的物质的量之比大于1:2,原因是反应过程中部分亚铁离子被氧气氧化为铁离子;(6)第2步反应FeOOH吸收CO,生成Fe3O4,化学方程式:6FeOOH+CO=2Fe3O4+CO2+3H2O ;其中氧化产物为CO2和还原产物Fe3O4的物质的量之比等于方程式中的计量数之比,为1:2;(7)纳米四氧化三铁的粒子大小在1纳米和100纳米之间纳米,Fe3O4投入分散剂中形成的分散系是胶体。
Fe3O4+4H2O ;(5)实际生产中为提高产率,起始所用FeSO4·7H2O和FeCl3·6H2O的物质的量之比大于1:2,原因是反应过程中部分亚铁离子被氧气氧化为铁离子;(6)第2步反应FeOOH吸收CO,生成Fe3O4,化学方程式:6FeOOH+CO=2Fe3O4+CO2+3H2O ;其中氧化产物为CO2和还原产物Fe3O4的物质的量之比等于方程式中的计量数之比,为1:2;(7)纳米四氧化三铁的粒子大小在1纳米和100纳米之间纳米,Fe3O4投入分散剂中形成的分散系是胶体。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。其部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 ②易分解:SO2Cl2 |
回答下列问题:
Ⅰ.实验室合成硫酰氯要先制取干燥氯气。制备干燥纯净的氯气所用仪器如下图:

(1)圆底烧瓶中发生的离子反应方程式为_____________。
(2)上述仪器的连接顺序是:e接 , 接 , 接 , 接 (按气流方向,用小写字母表示)。______________________
II.催化合成硫酰氯的实验装置如下图 (夹持仪器已省略):

(3)仪器B冷却水的进口为________(填“a””或“b”),活性炭的作用是________。
(4)装置D除干燥气体外,另一作用是_______________。若缺少D,则硫酰氯会水解,该反应的化学方程式为________________。
(5)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么? _______