题目内容
15.钢铁在潮湿的空气中容易发生电化学腐蚀,发生腐蚀时,负极电极反应式是Fe-2e-=Fe2+;CH4-O2的酸性燃料电池,电池工作时,正极电极反应式是O2+4e-+4H+=2H2O;电解精炼铜时,粗铜放在电解池的阳极;架设在海水中的石油钻井的钢铁设备,通常采用外加电流的阴极保护法保护,该钢铁设备作为阴极.分析 钢铁在潮湿的空气中发生电化学腐蚀,Fe易失电子生成亚铁离子而作负极;甲烷、氧气酸性燃料电池中,负极上甲烷失电子生成二氧化碳和氢离子,正极上氧气得电子和氢离子反应生成水;电解精炼粗铜时,粗铜作阳极、纯铜作阴极;作原电池正极或电解池阴极的电极被保护.
解答 解:钢铁在潮湿的空气中发生电化学腐蚀,Fe易失电子生成亚铁离子而作负极,电极反应式为Fe-2e-=Fe2+;甲烷、氧气酸性燃料电池中,负极上甲烷失电子生成二氧化碳和氢离子,正极上氧气得电子和氢离子反应生成水,电极反应式为O2+4e-+4H+=2H2O;电解精炼粗铜时,粗铜作阳极、纯铜作阴极,所以粗铜放在电解池的阳极;作原电池正极或电解池阴极的电极被保护,则架设在海水中的石油钻井的钢铁设备,通常采用外加电流的阴极保护法保护,该钢铁设备作为阴极,
故答案为:Fe-2e-=Fe2+;O2+4e-+4H+=2H2O;阳;阴.
点评 本题考查金属腐蚀与防护,明确原电池及电解池原理是解本题关键,知道常见防止金属腐蚀方法,难点是燃料电池电极反应式的书写,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.全氟丙烷(C3F8)是一种比二氧化碳有效104倍的“超级温室气体”.有关全氟丙烷的说法正确的是( )
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 全氟丙烷的电子式为: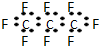 | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 全氟丙烷分子中既有极性键又有非极性键 |
7.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 22.4LCO和CO2的混合气体中所含的碳原子数一定是NA | |
| B. | 标况下,22.4L氦气所含原子数为2NA | |
| C. | 常温常压下,32gO2和32gO3所含氧原子数都是2NA | |
| D. | 常温下5.6g铁投入到足量浓硝酸中反应,转移电子数为0.3NA |
4.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,15g乙烷分子中含有的碳氢键数目为3NA | |
| B. | 标准状态下,22.4L的苯的分子数为NA | |
| C. | 通常状态下,1.7g的NH3中含有中子数为NA | |
| D. | 23gNa放入水中反应后共失去电子2NA |
5.翡翠是由X、Y、Z、W四种短周期元素组成的矿物,可表示为XY[Z2W6],X、Y、W元素的简单离子的电子层结构相同,X的原子半径比Y的大,Z的单质是常见的半导体材料,W是地壳中含量最多的元素.下列说法不正确的是( )
| A. | Y在化合物中显+3价 | |
| B. | X与W只能形成一种化合物 | |
| C. | W的简单氢化物稳定性比Z的强 | |
| D. | X的最高价氧化物对应的水化物碱性比Y的强 |
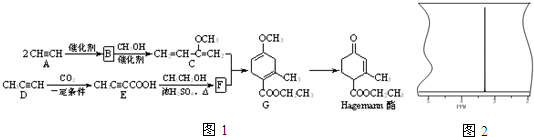
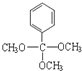 .
.
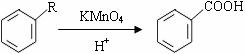
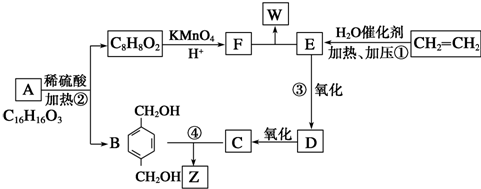
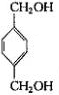 +2CH3COOH$→_{△}^{浓硫酸}$
+2CH3COOH$→_{△}^{浓硫酸}$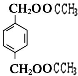 +2H2O.
+2H2O. ,
,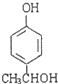 ,
,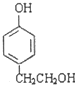 .
.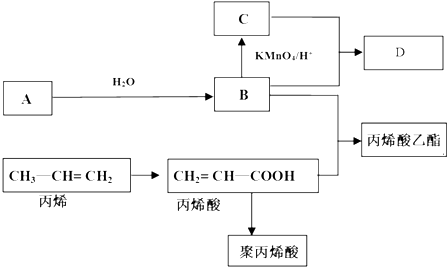
 CH2=CH-COOC2H5+H2O反应类型:酯化反应或取代反应
CH2=CH-COOC2H5+H2O反应类型:酯化反应或取代反应