题目内容
13.短周期元素X、Y、Z,在周期表中的位置如图所示,则下列说法错误的是( )
| A. | X单质最稳定 | B. | Y的氢化物为HY | ||
| C. | Z单质常温下是淡黄色固体 | D. | 能生成HXO |
分析 由短周期元素的位置,可知X为He元素,Y为F元素,Z为S元素,结合元素化合物性质解答.
解答 解:由短周期元素的位置,可知X为He元素,Y为F元素,Z为S元素.
A.X为He,原子最外层为稳定结构,性质最稳定,故A正确;
B.Y为F元素,其氢化物为HF,故B正确;
C.Z为S元素,其单质常温下是淡黄色固体,故C正确;
D.X为He,不能形成HHeO,故D错误,
故选:D.
点评 本题考查位置结构性质的相互关系应用,题目难度不大,注意对基础知识的理解掌握.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
4. 右图是可逆反应N2(g)+3H2(g)═2NH3(g) 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是( )
右图是可逆反应N2(g)+3H2(g)═2NH3(g) 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是( )
 右图是可逆反应N2(g)+3H2(g)═2NH3(g) 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是( )
右图是可逆反应N2(g)+3H2(g)═2NH3(g) 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是( )| A. | t1时,v正>v逆 | B. | t2时,反应到达限度 | ||
| C. | t2-t3,反应停止 | D. | t2-t3,各物质的浓度不再发生变化 |
1.下列物质能和甲烷反应的是( )
| A. | 酸性高猛酸钾 | B. | NaOH | C. | 氯气 | D. | 浓硫酸 |
8.(1)下表示元素周期表的一部分
①写出元素符号:fSi;hCl;
②c、d、e、b的原子半径由大到小的顺序是Na>Mg>Al>F;
③g、h的最高价氧化物的水化物中酸性强的是HClO4;
④a、f的氢化物中稳定性强的是SiH4.
⑤a元素和氢元素形成的化合物的电子式是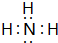 .
.
⑥c元素和b元素形成的化合物中含有的化学键类型是离子键.
(2)下表是元素周期表的一个片段,各元素均属于短周期元素
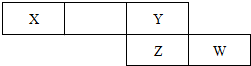
①若X的单质为空气的主要成分之一,则W的原子结构示意图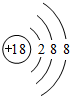 ;
;
②若Y能与钠形成反应生成淡黄色固体,则该淡黄色固体的化学式为Na2O2;含有的化学键类型有离子键、共价键.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | h | i |
②c、d、e、b的原子半径由大到小的顺序是Na>Mg>Al>F;
③g、h的最高价氧化物的水化物中酸性强的是HClO4;
④a、f的氢化物中稳定性强的是SiH4.
⑤a元素和氢元素形成的化合物的电子式是
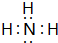 .
.⑥c元素和b元素形成的化合物中含有的化学键类型是离子键.
(2)下表是元素周期表的一个片段,各元素均属于短周期元素

①若X的单质为空气的主要成分之一,则W的原子结构示意图
 ;
;②若Y能与钠形成反应生成淡黄色固体,则该淡黄色固体的化学式为Na2O2;含有的化学键类型有离子键、共价键.
5.相同的甲、乙两容器中,一个充满C2H4,另一个充满C2H2和C2H6.在同温同压下,两个容器内的气体一定具有相同的( )
| A. | 原子总数 | B. | 分子总数 | C. | 质量 | D. | 密度 |
2.下列叙述正确的是( )
| A. | 金属镁工业冶炼的方法是采用直接加热分解法 | |
| B. | 石油是由多种碳氢化合物组成的混合物 | |
| C. | 煤的主要成分是碳单质 | |
| D. | 酸雨的形成主要是由于CO2含量过高 |
3.在溶液中含有的物质至少有( )
| A. | 一种 | B. | 两种 | C. | 三种 | D. | 四种 |
