题目内容
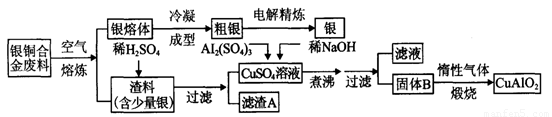
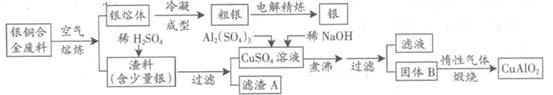
银铜合金广泛用于航空工业.从切割废料中回收银并制备铜化工产品的工艺如图: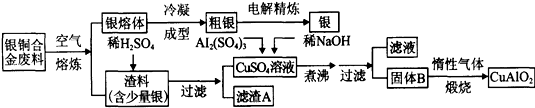
(1)电解精练银时,阴极反应式为
(2)固体混合物B的组成为
(3)煅烧过程中生成的氧化产物与NH3在催化剂条件下反应的化学方程式为
(4)若银铜合金中铜的质量分数为64%,理论上3.0kg废料中的铜可完全转化为
分析:(1)根据电解原理分析判断;无色的NO在常温下与空气中的O2迅速化合生成红棕色N02;
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Cu(OH)2分解的温度为80℃判断产物;根据氢氧化铝显两性能与碱反应;
(3)煅烧过程中生成的氧化产物是氧气,NH3在催化剂条件下和氧气反应生成NO和水;NO和氧气和水能反应生成硝酸,硝酸和氨气反应生成硝酸铵;
(4)根据铜元素守恒建立关系式:Cu~CuAlO2来计算;根据铝元素守恒建立关系式:Al2(SO4)3~2CuAlO2来计算.
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Cu(OH)2分解的温度为80℃判断产物;根据氢氧化铝显两性能与碱反应;
(3)煅烧过程中生成的氧化产物是氧气,NH3在催化剂条件下和氧气反应生成NO和水;NO和氧气和水能反应生成硝酸,硝酸和氨气反应生成硝酸铵;
(4)根据铜元素守恒建立关系式:Cu~CuAlO2来计算;根据铝元素守恒建立关系式:Al2(SO4)3~2CuAlO2来计算.
解答:解:(1)电镀法精炼银时,粗银为阳极,精银为阴极,阳极上失电子变成离子进入溶液了:Ag-e-=Ag+,阴极银离子得到电子形成单质银:Ag++e-=Ag;生成红棕色气体是N02,N02与水反应的化学方程式为:3NO2+H2O=2HNO3+NO↑,故答案为:Ag++e-=Ag;3NO2+H2O=2HNO3+NO↑;
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Al(OH)3和Cu(OH)2,煮沸后Cu(OH)2分解产生氧化铜,可知B为Al(OH)3和CuO;氢氧化铝显两性能与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O,故答案为:Al(OH)3和CuO;Al(OH)3+OH-=AlO2-+2H2O;
(3)Cu化合价由+2变为+1,Al化合价没变,因此O的化合价升高,得到氧化产物是氧气,NH3在催化剂条件下和氧气反应生成NO和水,化学方程式为:4NH3+5O2
4NO+6H2O,NO和氧气和水能反应生成硝酸,硝酸和氨气反应生成硝酸铵,现象为产生白烟,
故答案为:4NH3+5O2
4NO+6H2O;NH4NO3;
(4)由关系式:Cu~CuAlO2得n(CuAlO2)=
=30mol,则CuAlO2为30mol,由关系式:Al2(SO4)3~2CuAlO2得Al2(SO4)3=n(CuAlO2)×
=15mol,所以需要体积为
=15L,
故答案为:30;15.
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Al(OH)3和Cu(OH)2,煮沸后Cu(OH)2分解产生氧化铜,可知B为Al(OH)3和CuO;氢氧化铝显两性能与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O,故答案为:Al(OH)3和CuO;Al(OH)3+OH-=AlO2-+2H2O;
(3)Cu化合价由+2变为+1,Al化合价没变,因此O的化合价升高,得到氧化产物是氧气,NH3在催化剂条件下和氧气反应生成NO和水,化学方程式为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(4)由关系式:Cu~CuAlO2得n(CuAlO2)=
| 3000g×64% |
| 64g/mol |
| 1 |
| 2 |
| 15mol |
| 1.0mol?L-1 |
故答案为:30;15.
点评:本题以从废料中回收银并制备铜化工产品为背景,考查了电解原理、沉淀的判断、氧化还原反应的配平以及化学计算,难度不大.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
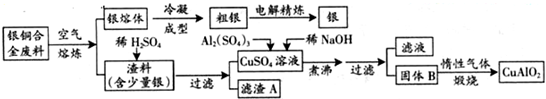
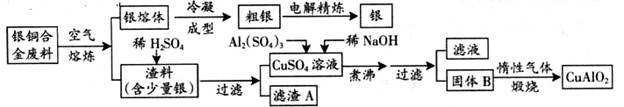
 CuAlO2 + ↑。
CuAlO2 + ↑。