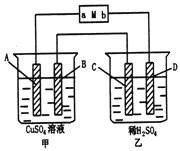
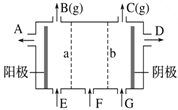
��Ŀ����
����Ŀ����11.2g��Mg��Cu�������ȫ�ܽ��������������У��ռ���Ӧ����������x���ٶ�����������ȫ���ݳ���������������Һ�м���������NaOH��Һ������21.4g���������������ƶ�����x�ijɷֿ�����
A. 0.3mol NO2��0.3mol NO
B. 0.2mol NO2��0.1mol N2O4
C. 0.6mol NO
D. 0.1mol NO��0.2mol NO2��0.05mol N2O4
���𰸡�D
����������Mg-Cu����������������ᷴӦ������Һ�м���������NaOH��Һ������21.4g����Ϊ������þ��������ͭ�����Գ�����������������Ϊ21.4g-11.2g=10.2g�����ʵ���Ϊ![]() =0.6mol�����ݵ���غ��֪��11.2g��Mg-Cu�ṩ�ĵ���Ϊ0.6mol��A������0.3mo1NO2��0.3mo1NO��NԪ�ػ�õ���Ϊ0.3mol����5-4��+0.3mol����5-2��=1.2mol����ʧ���Ӳ���ȣ�ѡ��A����B������0.2mo1NO2��0.1mo1N2O4��NԪ�ػ�õ���Ϊ0.2mol����5-4��+0.1mol��2����5-4��=0.4mol����ʧ���Ӳ���ȣ�ѡ��B����C������0.6molNO��NԪ�ػ�õ���Ϊ0.6mol����5-2��=1.8mol��ѡ��C����D������0.1mol NO��0.2mol NO2��0.05mol N2O4��NԪ�ػ�õ���Ϊ0.1mol����5-2��+0.2mol����5-4��+0.05mol��2����5-4��=0.6mol����ʧ������ȣ�ѡ��D��ȷ����ѡB��
=0.6mol�����ݵ���غ��֪��11.2g��Mg-Cu�ṩ�ĵ���Ϊ0.6mol��A������0.3mo1NO2��0.3mo1NO��NԪ�ػ�õ���Ϊ0.3mol����5-4��+0.3mol����5-2��=1.2mol����ʧ���Ӳ���ȣ�ѡ��A����B������0.2mo1NO2��0.1mo1N2O4��NԪ�ػ�õ���Ϊ0.2mol����5-4��+0.1mol��2����5-4��=0.4mol����ʧ���Ӳ���ȣ�ѡ��B����C������0.6molNO��NԪ�ػ�õ���Ϊ0.6mol����5-2��=1.8mol��ѡ��C����D������0.1mol NO��0.2mol NO2��0.05mol N2O4��NԪ�ػ�õ���Ϊ0.1mol����5-2��+0.2mol����5-4��+0.05mol��2����5-4��=0.6mol����ʧ������ȣ�ѡ��D��ȷ����ѡB��