��Ŀ����
����Ŀ��±���������������о��й㷺��Ӧ�ã��ش��������⣺
(1)��һ�ֶ��ȴ�����Ϊ�����л��ܼ�������ӽṹΪ�������壬����______(д��ѧʽ)
(2)���ķ���ϩ�ȶ��������Dz�ճ����Ϳ�㣬���Ľṹ��ʽ��________________
(3)��֪�Ҷ����������ᣬ�ڹ�ҵ���й㷺����;���������кϳ�·����գ�

�ֱ�д����Ӧ�ڢ۵Ļ�ѧ��Ӧ����ʽ��________��_____________��
(4)��Ҫ������������⣺�� �ٱ� ���Ҵ� �ۼױ� �������� ��![]() ��
��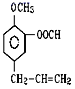 ��
��![]() ����������(����)��
����������(����)��
���ܺͽ����Ʒ�Ӧ�ų�H2����________��
�ڳ�����������ˮ��ѧ��Ӧ����________��
����ʹ����KMnO4��Һ��ɫ����________��
���𰸡�CCl4 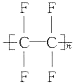 CH2ClCH2Cl+2NaOH��CH2OHCH2OH+2NaCl CH2OHCH2OH +O2��CHOCHO+2H2O �ڢ� �ݢޢ� �ڢۢݢޢ�
CH2ClCH2Cl+2NaOH��CH2OHCH2OH+2NaCl CH2OHCH2OH +O2��CHOCHO+2H2O �ڢ� �ݢޢ� �ڢۢݢޢ�
��������
(1) ���ȴ������з��ӽṹΪ���������Ϊ���Ȼ�̼������ʽΪCCl4��
(2) ���ķ���ϩΪ�ķ���ϩ��CF2=CF2���ļӾ۲���ṹ��ʽΪ ��
��
(3) ��Ӧ��Ϊ±������ˮ�⣬����ʽΪ��CH2ClCH2Cl+2NaOH��CH2OHCH2OH+2NaCl��
��Ӧ��Ϊ�ǻ�����������ȩ��������ʽΪ��CH2OHCH2OH +O2��CHOCHO+2H2O��
(4) ���ܺͽ����Ʒ�Ӧ�ų�H2���л��ﺬ���ǻ����Ȼ�����ѡ�ڢݣ�
�� ������������ˮ�����ӳɷ�Ӧ���л���Ӧ�ú���̼̼˫����̼̼�����������������Тޣ����߷��ǻ��ڶ�λ����ȡ����Ӧ�������������Тݣ����߷���������Ӧ������ȩ�����Ա����������������Ǣߣ���ѡ�ݢޢߣ�
�� ��ʹ����KMnO4��Һ��ɫ���л��ﺬ���ǻ���ȩ����̼̼˫����ױ�����ѡ�ڢۢݢޢߡ�

����Ŀ������֪���볣���жϣ����й���SO2��Na2CO3��aq����Ӧ�����ӷ���ʽ����д�У����������ǣ� ��
�� | ���볣�� |
̼�� | K1��4��10��7 K2��5.6��10��11 |
������ | K1��1.54��10��2 K2��1.02��10��7 |
A.SO2��H2O��2CO32��=2HCO3����SO32��
B.SO2��H2O��CO32��=H2O+CO2��SO32��
C.2SO2��2H2O��CO32��=H2O+CO2��2HSO3��
D.SO2��H2O��CO32��=HCO3����HSO3��
����Ŀ��������һ����Ҫ����ԭ�ϡ�
(1)�¹���ѧ�ҹ�����1902�꿪ʼ�о��ɵ���������ֱ�Ӻϳɰ���
��֪����![]() ��H=a kJ/mol
��H=a kJ/mol
��ÿ�ƻ�lmol�йػ�ѧ����Ҫ���������±���
H-H | N-H | N��N |
436kJ | 391kJ | 946k |
��a=_________________��
(2)��ͼΪ��ͬ�¶�(T)����ͬͶ�ϱ�[n(![]() )/n(
)/n(![]() )]ʱ��Ӧ�ﵽƽ��ʱ
)]ʱ��Ӧ�ﵽƽ��ʱ![]() ��ת���ʱ仯���ߡ�
��ת���ʱ仯���ߡ�

��![]() ��
��![]() ��
��![]() ��
��![]() �Ĵ�С��ϵΪ__________________��
�Ĵ�С��ϵΪ__________________��
�ڱ����¶Ⱥ�������䣬���Ͷ�ϱ�[n(![]() )/n(
)/n(![]() )]�������´ﵽƽ��ʱ������˵��һ����ȷ����_______(����ĸ���)��
)]�������´ﵽƽ��ʱ������˵��һ����ȷ����_______(����ĸ���)��
A.![]() ��Ũ������
��Ũ������
B.![]() ��ת��������
��ת��������
C.![]() �������������
�������������
D.![]() ��Ũ�ȼ�С
��Ũ�ȼ�С
���¶�Ϊ![]() ʱ����2L�ܱ������м���1.0mol
ʱ����2L�ܱ������м���1.0mol![]() ��1.0mol
��1.0mol![]() ����5min��Ӧ�ﵽƽ�⣬����v(
����5min��Ӧ�ﵽƽ�⣬����v(![]() )��ʾ�÷�Ӧ��ƽ������Ϊ____________________����Ӧ��
)��ʾ�÷�Ӧ��ƽ������Ϊ____________________����Ӧ��![]() ʱ��ƽ�ⳣ��K=________________��
ʱ��ƽ�ⳣ��K=________________��
(3)һ�����ͳ������е�������ķ����Dz���![]() ����ԭ����ԭ�����еĵ��������Ҳ�������Ⱦ��д��
����ԭ����ԭ�����еĵ��������Ҳ�������Ⱦ��д��![]() ��ԭ
��ԭ![]() �Ļ�ѧ��Ӧ����ʽ_____________________________________��
�Ļ�ѧ��Ӧ����ʽ_____________________________________��
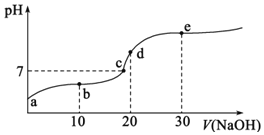
(4)���ñ�����ⶨijϡ��ˮ��Ũ�ȣ�Ӧѡ��__________��ָʾ�����ζ��������۾�ע��_____________����֪ϡ��ˮ���Ϊ25.0mL���ζ������������0.0100mol/L�����ƽ�����Ϊ20.0mL����ð�ˮ��Ũ��Ϊ________________(����2λ��Ч����)�����ζ�ǰ�ζ��ܼ��������ݣ��ζ�����������ݣ���ⶨ���________(�ƫ����ƫС���������䡱)��