题目内容
水是生命之源,与人类的生活密切相关。在化学实验和科学研究中,水有多种用途。
(1)下列说法中正确的是 (填序号)。
| A.每一个水分子内含有两个氢键 |
| B.水分子间存在范德华力,所以水分子稳定 |
| C.分子间形成的氢键使水的熔点和沸点升高 |
| D.冰熔化时水分子内共价键发生断裂 |
(3)水分子在特定条件下易形成水合氢离子(H3O+)。其中含有的化学键为 。
(4)如果需要增大水的电离程度,除了升高温度外,还可以采用的方法有 (回答一种即可)。若室温时,将某一元酸HA加水配成0.1 mol·L-1的稀溶液,此时HA在水中有0.1%发生电离,则由HA电离出的c(H+)约为水电离出的c(H+)的 倍。
(5)将一定量的Na2SO3固体溶于水,所得溶液中的电荷守恒关系式为 。
(6)研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差异进行发电。已知该电池用金属银做负极,正极反应为5MnO2 +2Na++2e-
 Na2Mn5O10,请写出电池总反应式 。
Na2Mn5O10,请写出电池总反应式 。
(1)C(2分)
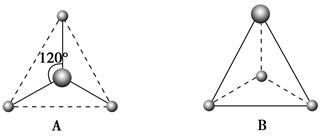
(2)V形(2分)
(3)极性键、配位键(2分)
(4)加入可水解的盐(或答具体的物质) 106 (各2分,共4分)
(5)c(Na+)+c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-) (2分)
(6)5MnO2 +2Ag +2NaCl  Na2Mn5O10+2AgCl (2分)
Na2Mn5O10+2AgCl (2分)
解析试题分析:(1)氢键存在于水分子之间,故A错误;水分子稳定和范德华力无关,跟水分子内部的共价键有关,故B错误;C正确,冰融化属于物理变化,破坏的是分子间作用力,共价键没有发生变化,故D错误;
(2)水分子中氧原子含有2个σ键和2个孤对电子,所以水分子是V型结构;
(3)水合氢离子(H3O+)中含有的化学键为极性键、配位键;
(4)水的电离是吸热反应,升高温度促进水电离,酸或碱抑制水电离,含有弱根离子的盐促进水电离;HA电离出的c(H+)为0.1mol·L-1×0.1%=10-4mol·L-1,水电离产生的氢离子浓度为10-10mol·L-1,则由HA电离出的c(H+)约为水电离出的c(H+)的106倍;
(5)Na2SO3溶液中存在水解平衡:SO32-+H2O HSO3-+OH-,HSO3-+H2O
HSO3-+OH-,HSO3-+H2O H2SO3+OH-,所得溶液中的电荷守恒关系式为c(Na+)+c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-);
H2SO3+OH-,所得溶液中的电荷守恒关系式为c(Na+)+c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-);
(6)负极发生反应的电极方程式为:Ag+Cl--e-=AgCl,负极发生反应的电极方程式加上正极发生反应的电极方程式,就得到总反应方程式,5MnO2 +2Ag +2NaCl  Na2Mn5O10+2AgCl。
Na2Mn5O10+2AgCl。
考点:考查关于水的综合化学知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列说法正确的是
| A.含有离子键的化合物一定是离子化合物 |
| B.含有共价键的化合物一定是共价化合物 |
| C.所有物质都含有共价键 |
| D.均由非金属元素形成的化合物不可能是离子化合物 |
图形因表达准确且信息量大而得到广泛应用。请根据所给图形回答下列问题:
(1)如下图表示容器中气体粒子的示意图,图中“”和“”分别代表不同元素的原子,它们的结合体代表分子,则图中可表示氮气的是(填字母,下同)________,含有________共价键(填“极性”或“非极性”),可表示氯化氢(HCl)分子的是________,含有________共价键(填“极性”或“非极性”),可表示一氧化碳和氧气的混合气体的是________含有________共价键(填“极性”或“非极性”)。
(2)下图是水分子在一定条件下分解的示意图,从中获得的信息不正确的是________。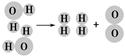
| A.生成1 mol O2需断开4 mol H—O共价键 |
| B.水分解后生成氢气和氧气的分子数比为2∶1 |
| C.水分解过程中,分子的种类不变 |
| D.水分解过程中,原子的数目不变 |
硫元素可以形成多种物质如 、SO2、SO32-、SO42-等。
、SO2、SO32-、SO42-等。
(1) 中S原子的轨道杂化类型是 ,
中S原子的轨道杂化类型是 , 的空间构型是 。
的空间构型是 。
(2)向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成。分析表明该沉淀中Cu、S、N的物质的量之比为1:1:1,经测定该沉淀的晶体里有一种三角锥型的阴离子和一种正四面体型的阳离子。
①[Cu(NH3)4]SO4中Cu2+的电子排布式为 。
②[Cu(NH3)4]SO4中存在的化学键类型有 (填序号)。
| A.共价键 | B.氢键 | C.离子键 | D.配位键 E.分子间作用力 |
下列物质的晶体属于分子晶体的是
| A.Si | B.CO2 | C.NaCl | D.Cu |
下列各组物质中,按熔点由低到高排列正确的是( )
| A.O2、I2、Hg | B.CO2、KCl、SiO2 |
| C.HF、HCl、HI | D.SiO2、NaCl、SO2 |