题目内容
3.美国墨西哥湾英国石油公司的一海上石油钻探平台发生爆炸,大量石油泄漏,给墨西哥湾海域带来巨大的经济损失和生态灾难.下列关于石油加工的叙述中,错误的是( )| A. | 石油分馏所得的馏分是一种具有固定熔、沸点的纯净物 | |
| B. | 石油裂化的主要目的是提高汽油等轻质油的产量 | |
| C. | 石油裂解的原料是石油分馏产物,包括石油气 | |
| D. | 石油在催化剂的作用下加热,可以使链状烃转化为环状烃(如苯、甲苯等) |
分析 A.石油的分馏所得的馏分仍是混合物;
B.石油的裂化的主要目的是提高汽油等轻质油的产量;
C.石油裂解的原料是重油;
D.根据石油的催化重整来分析.
解答 解:A.石油的分馏所得的馏分仍是多种烷烃和环烷烃的混合物,没有固定熔沸点,故A错误;
B.石油的裂化的主要目的是提高汽油等轻质油的产量,裂解的目的是获得乙烯,故B正确;
C.石油裂解的原料是重油,故C错误;
D.石油在加热和催化剂的作用下,可以通过结构的重新调整,使链状烃转化为环状烃,如苯或甲苯,此为石油的催化重整,故D正确.
故选AC.
点评 本题考查了石油的综合利用,重点掌握石油的裂化和裂解的目的,此为考试的热点,难度不大.

练习册系列答案
相关题目
3. 已知某碱性硼化矾(VB2)-空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3.以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
已知某碱性硼化矾(VB2)-空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3.以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
 已知某碱性硼化矾(VB2)-空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3.以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
已知某碱性硼化矾(VB2)-空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3.以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )| A. | VB2电极发生的电极反应为:2VB2+11H2O-22e-═V2O5+2B2O3+22H+ | |
| B. | 若B装置内的液体体积为400mL,则CuSO4溶液的物质的量浓度为0.025mol/L | |
| C. | 电解过程中,b电极表面先有红色物质析出,然后有气泡产生 | |
| D. | 外电路中电子由a电极流向b电极 |
4.煤、石油、天然气是重要的能源和化工原料,下列说法正确的是( )
| A. | 石油裂解得到的汽油是纯净物 | |
| B. | 石油产品都可用于聚合反应 | |
| C. | 煤的干馏可以得到甲烷、苯和氨等重要化工原料 | |
| D. | 直馏汽油可以使溴的四氯化碳溶液褪色 |
11.下列物质的焰色反应实验,透过蓝色钴玻璃观察到火焰呈紫色的是( )
| A. | KCl | B. | CuCl2 | C. | CaCl2 | D. | NaCl |
18.下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
| A. | 2.4 g金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1 mol HCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 | |
| C. | 在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10NA | |
| D. | 22.4 L的CO气体与l mol N2所含的电子数相等 |
8.NO和CO都是汽车尾气里的有害物质,它们能缓慢地反应生成氮气和二氧化碳气体:2NO(g)+2CO(g)?N2(g)+2CO2(g).对此反应,下列叙述正确的是( )
| A. | 使用催化剂能加快反应速率 | |
| B. | 压强增大正反应速率增大,逆反应速率减小 | |
| C. | 冬天气温低,反应速率降低,对人体危害较小 | |
| D. | 无论外界条件怎样改变,均对此化学反应的速率无影响 |
15.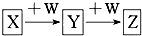 X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图所示转化关系(其他产物已略):下列说法不正确的是( )
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图所示转化关系(其他产物已略):下列说法不正确的是( )
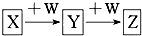 X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图所示转化关系(其他产物已略):下列说法不正确的是( )
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图所示转化关系(其他产物已略):下列说法不正确的是( )| A. | 若W是单质铁,则Z溶液可能是FeCl2溶液 | |
| B. | 若X是金属铝,则W可能是强碱 | |
| C. | 若W是氢氧化钠,则X与Z可能反应生成Y | |
| D. | 若X为氧气,则X与Y的相对分子质量可能相差12 |
13.将几种铁的氧化物的混合物加入100mL、7mol•L-1的盐酸中.氧化物恰好完全溶解,在所得的溶液中通入0.56L(标准状况)氯气时,恰好使溶液中的Fe2+完全转化为Fe3+,则该混合物中铁元素的质量分数为( )
| A. | 72.4% | B. | 71.4% | C. | 79.0% | D. | 63.6% |