题目内容
短周期元素R的原子核外电子数等于核内中子数,该元素单质7.2g与氧气充分反应可生成12g化合物RO,则该元素的价电子层是( )
| A.1s2 | B.2s2 | C.3s2 | D.4s2 |

 C
C根据质量守恒定律可知,参加反应的氧气质量是4.8g,物质的量是0.15mol,得到电子的物质的量是0.15mol×4=0.6mol。根据化学式可知,R的化合价是+2价,所以根据电子的得失守恒可知,R的物质的量是0.6mol÷2=0.3mol,所以R的相对原子质量是7.2÷0.3=24,即R是Mg,所以根据构造原理可知,镁元素的价电子层是3s2,答案选C。

练习册系列答案
相关题目
 ZX2反应生成一种化合
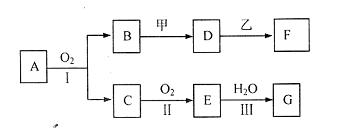
ZX2反应生成一种化合 物Y2ZX3,已知三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,Z原子的最外层电子数是次外层电子数的2倍。试回答:
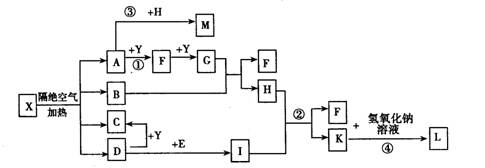
物Y2ZX3,已知三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,Z原子的最外层电子数是次外层电子数的2倍。试回答: 原子数之比为2∶1的化合物X和1∶1的化合物Y,D与B也能组成原子数之比为2:1的化合物M和1:1的化合物Z;1molC单质跟X反应放出0.5mol气体B2,1molD单质跟X反应放出11.2L(标准)气体A2,1molZ化合物跟X反应放出0.5mol气体B2。试回答:
原子数之比为2∶1的化合物X和1∶1的化合物Y,D与B也能组成原子数之比为2:1的化合物M和1:1的化合物Z;1molC单质跟X反应放出0.5mol气体B2,1molD单质跟X反应放出11.2L(标准)气体A2,1molZ化合物跟X反应放出0.5mol气体B2。试回答: