题目内容
2006年10月16日美国与俄罗斯宣布,两国科学家合作成功合成了118号超重元素。对118号元素下列叙述合理的是
| A.它的最外层电子数是8 | B.它属于第VIII族 |
| C.它是活泼的金属元素 | D.它的中子数是118 |
A
解析试题分析:118号元素应位于元素周期表的第七周期0族,所以最外层电子数是8,它属于非金属,中子数无法判断,所以答案选A。
考点:考查由原子序数判断原子结构、在元素周期表的位置

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
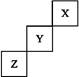
4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8,下列说法不正确的是
| A.与W相邻的同主族元素可制成重要的半导体材料 |
| B.元素原子半径从大到小的顺序是X、Y、Z |
| C.WZ4分子中W、Z原子通过共价键结合且最外层均达到8电子结构 |
| D.W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是H2YO4 |
依据元素周期表及元素周期律,下列推断中正确的是
| A.同一周期元素的原子,半径越小越容易失去电子 |
| B.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| C.向氢硫酸溶液中滴入氯水有单质硫生成,可以验证硫元素的非金属性比氯元素弱 |
| D.主族元素的最高正化合价等于该元素原子的核外电子数 |
在下列元素中,原子半径最小的是
| A.C | B.N | C.O | D.F |
下列性质的递变中,正确的是
| A.O、S、Na的原子半径依次增大 |
| B.HF、NH3、SiH4的稳定性依次增强 |
| C.LiOH、KOH、CsOH的碱性依次增强 |
| D.HCl、HBr、HI的还原性依次减弱 |
铋(Bi)在医药方面有重要应用。下列关于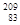 Bi和
Bi和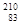 Bi的说法正确的是( )
Bi的说法正确的是( )
A.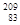 Bi和 Bi和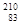 Bi都含有83个中子 Bi都含有83个中子 |
B.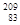 Bi和 Bi和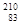 Bi互为同位素 Bi互为同位素 |
C.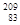 Bi和 Bi和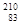 Bi的核外电子数不同 Bi的核外电子数不同 |
D.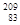 Bi和 Bi和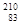 Bi分别含有126和127个质子 Bi分别含有126和127个质子 |
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )。
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.L2+与R2-的核外电子数相等
B.M与T形成的化合物既能与酸反应又能与强碱反应
C.氢化物的稳定性为H2T<H2R
D.单质与浓度相等的稀盐酸反应的速率为Q>L
(双选)酸根离子R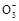 所含电子数比硝酸根离子N
所含电子数比硝酸根离子N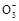 所含的电子数多10个,则下列说法正确的是( )。
所含的电子数多10个,则下列说法正确的是( )。
| A.R原子的电子层数比氮原子的电子层数多1 |
B.酸根离子R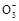 中R的化合价与硝酸根离子N 中R的化合价与硝酸根离子N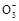 中N的化合价相等 中N的化合价相等 |
C.R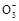 和N 和N 只能被还原,不能被氧化 只能被还原,不能被氧化 |
| D.R原子和氮原子的最外层电子数相同 |