题目内容
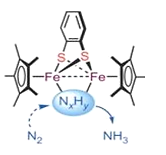
【题目】生物固氮与模拟生物固氮都是重大基础性研究课题。大连理工大学曲景平教授团队设计合成了一类新型邻苯二硫酚桥联双核铁配合物,建立了双铁分子仿生化学固氮新的功能分子模型。如图是所发论文插图。以下说法错误的是
A.催化剂不能改变反应的焓变
B.催化剂不能改变反应的活化能
C.图中反应中间体NXHY数值X<3
D.图示催化剂分子中包含配位键
【答案】B
【解析】
A.催化剂能够改变反应途径,不能改变反应物、生成物的能量,因此不能改变反应的焓变,A正确;
B.催化剂能够改变反应途径,降低反应的活化能,B错误;
C.在过渡态,氮气分子可能打开叁键中部分或全部共价键,然后在催化剂表面与氢原子结合形成中间产物,故x可能等于1或2,C正确;
D.根据图示可知,在中间体的Fe原子含有空轨道,在S原子、N原子上含有孤对电子,Fe与S、N原子之间通过配位键连接,D正确;
故合理选项是B。

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目