题目内容
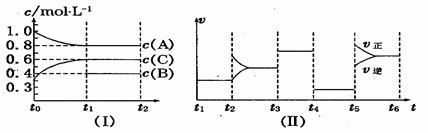
(16分)向一定体积的密闭器中加入2 mol A、0.6 mo1 C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图(Ⅰ)所示,其中t0~t1阶段c(B)未画出.图(Ⅱ)为t2时刻后改变反应条件,化学反应速率随时间变化的情况,四个阶段改变的条件均不相同,每个阶段只改变浓度、温度、压强、催化剂中的一个条件,其中t3~t4阶段为使用催化剂.
请回答下列问题:
(1)若t1=15 min,则t0~t1阶段以C物质的浓度变化表示反应速率为 。
(2) t4~t5阶段改变的条件为 ,B的起始物质的量浓度为 ,各阶段平衡时对应的平衡常数如下表所示:
则K1= (保留两位小数),
K1、K2、K3、K4、K5之间的关系为 (用“>”、“<”或“=”连接).
(3) t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为akJ,写出此温度下该反应的热化学方程式
。
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为 .

请回答下列问题:
(1)若t1=15 min,则t0~t1阶段以C物质的浓度变化表示反应速率为 。
(2) t4~t5阶段改变的条件为 ,B的起始物质的量浓度为 ,各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
K1、K2、K3、K4、K5之间的关系为 (用“>”、“<”或“=”连接).
(3) t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为akJ,写出此温度下该反应的热化学方程式
。
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为 .
(1)0.02mol/(L·min) (2)减压 0.5mol/L 0.84 K1=K2=K3=K4<K5
 (3) 2A(g)+B(g)?3C(g) △H=+200kJ/mol (4) a+2c/3=2.4 、b+c/3=1.2
(3) 2A(g)+B(g)?3C(g) △H=+200kJ/mol (4) a+2c/3=2.4 、b+c/3=1.2
 (3) 2A(g)+B(g)?3C(g) △H=+200kJ/mol (4) a+2c/3=2.4 、b+c/3=1.2
(3) 2A(g)+B(g)?3C(g) △H=+200kJ/mol (4) a+2c/3=2.4 、b+c/3=1.2(1)化学反应速率通常用单位时间内浓度的变化量来表示。根据图像I可知在15min内C的浓度变化量是0.6mol/L-0.3mol/L=0.3mol/L,所以速率为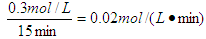
(2)由图像Ⅱ可知,在t4~t5阶段反应速率减小,但平衡不移动,所以改变的条件不可能是温度和浓度,由于在t3~t4阶段为使用催化剂,所以该阶段只是降低压强。这说明改变压强平衡不移动,因此反应前后体积是不变的。根据图像I可知A是反应物,C是生成物,二者的变化量之比是2︰3,所以要使反应前后体积不变,B只是反应物,及反应的方程式为2A+B 3C。C的浓度增加了0.3mol/L,则B的浓度减少了0.1mol/L,所以B的起始浓度是0.4mol/L+0.1mol/L=0.5mol/L。在t1~t2阶段平衡是ABC的浓度(mol/L)分别为0.8、0.4、0.6,所以平衡常数为
3C。C的浓度增加了0.3mol/L,则B的浓度减少了0.1mol/L,所以B的起始浓度是0.4mol/L+0.1mol/L=0.5mol/L。在t1~t2阶段平衡是ABC的浓度(mol/L)分别为0.8、0.4、0.6,所以平衡常数为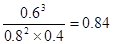 。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
(3)根据题意科判断,每消耗0.01molA,反应就吸收能量akJ,所以反应的热化学方程式为2A(g)+B(g)?3C(g) △H=+200kJ/mol。
(4)因为容器容积不变(容器容积是2L),所以要使平衡等效,则起始物质的物质的量是相等的。根据题意可知起始时AB的物质的量分别为2.4mol和1.2mol,则把cmol的C转化为AB,则AB的物质的量(mol)分别是a+2c/3、b+c/3,所以关系式必须满足a+2c/3=2.4、b+c/3=1.2.
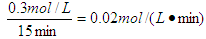
(2)由图像Ⅱ可知,在t4~t5阶段反应速率减小,但平衡不移动,所以改变的条件不可能是温度和浓度,由于在t3~t4阶段为使用催化剂,所以该阶段只是降低压强。这说明改变压强平衡不移动,因此反应前后体积是不变的。根据图像I可知A是反应物,C是生成物,二者的变化量之比是2︰3,所以要使反应前后体积不变,B只是反应物,及反应的方程式为2A+B
 3C。C的浓度增加了0.3mol/L,则B的浓度减少了0.1mol/L,所以B的起始浓度是0.4mol/L+0.1mol/L=0.5mol/L。在t1~t2阶段平衡是ABC的浓度(mol/L)分别为0.8、0.4、0.6,所以平衡常数为
3C。C的浓度增加了0.3mol/L,则B的浓度减少了0.1mol/L,所以B的起始浓度是0.4mol/L+0.1mol/L=0.5mol/L。在t1~t2阶段平衡是ABC的浓度(mol/L)分别为0.8、0.4、0.6,所以平衡常数为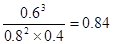 。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。(3)根据题意科判断,每消耗0.01molA,反应就吸收能量akJ,所以反应的热化学方程式为2A(g)+B(g)?3C(g) △H=+200kJ/mol。
(4)因为容器容积不变(容器容积是2L),所以要使平衡等效,则起始物质的物质的量是相等的。根据题意可知起始时AB的物质的量分别为2.4mol和1.2mol,则把cmol的C转化为AB,则AB的物质的量(mol)分别是a+2c/3、b+c/3,所以关系式必须满足a+2c/3=2.4、b+c/3=1.2.

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
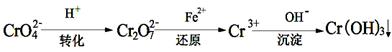
 Cr2O72- + H2O能说明反应到达平衡状态的是
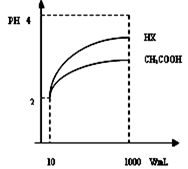
Cr2O72- + H2O能说明反应到达平衡状态的是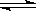 2HF
2HF 
 C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到该条件下的最大限度的是
C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到该条件下的最大限度的是 H2(气)+I2(气),达到平衡时,下列说法正确的是 ( )
H2(气)+I2(气),达到平衡时,下列说法正确的是 ( ) 3C(g),只有反应到达平衡时才一定具有的性质是
3C(g),只有反应到达平衡时才一定具有的性质是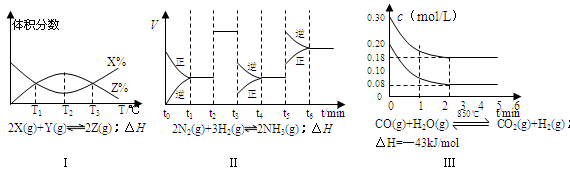
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
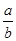 =__________
=__________