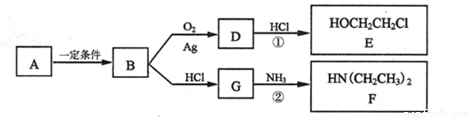
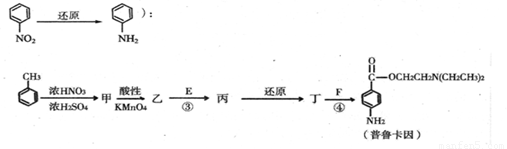
��Ŀ����
�����ֲ�ͬ�����ȵ�����ͭ��̿�۵Ļ������Ʒ�٢ڢۡ��ס��ҡ�����ͬѧ��ȡһ����Ʒ����ǿ�ȳ�ַ�Ӧ���ⶨ����Ʒ������ͭ������(1)��ȡ��Ʒ��ǿ�ȣ������ù���Ϊ����ͭ����������������ϡ�������ȣ�����?1.12 L?(��״��)���壬����Ʒ��������ͭ������Ϊ___________g��
(2)��ȡ��Ʒ��a gǿ�ȣ����ɵ����岻��ʹ�����ʯ��ˮ����ǡ��ٽ���Ӧ��Ĺ�����������ϡ�����ȣ���ַ�Ӧ����b g����ʣ�࣬��ʣ�����Ļ�ѧʽΪ____________________����Ʒ��������ͭ����Ϊ__________g(�Ժ�a��b�Ĵ���ʽ��ʾ)��
(3)��������Ʒ��ǿ�Ⱥ�ʣ��Ĺ��壬������ԭ��Ʒ������c g�����ù���Ϊ����ͭ������Ʒ��������ͭ���ʵ���(n)��ȡֵ��ΧΪ__________��
����:(1)��ʵ���з����ķ�ӦΪ��
3Cu+8HNO3====3Cu(NO3)2+2NO��+4H2O
�Ĺ�ϵΪCuO��Cu��![]() NO
NO
����ԭ�������CuO������Ϊ��![]() ��80 g��mol-1=6.0 g��
��80 g��mol-1=6.0 g��
(2)��ʵ���з����ķ�ӦΪ��
CuO+C====Cu+CO��
3Cu+8HNO3====3Cu(NO3)2+2NO��+4H2O
ʣ��Ĺ���ΪC������Ϊb g�����Է�Ӧ��ʵ������C��CuO��������Ϊ(a-b)g������CuO������Ϊ��![]() ��
��
(3)��ʵ�鷢���ķ�Ӧ����Ϊ��
CuO+C====Cu+CO�� ��
2CuO+C====2Cu+CO2�� ��
ǿ�Ⱥ������������c g��˵��������c g���塣
���ֻ������Ӧ�٣�����c g CO���壬��CuO�����ʵ���Ϊ![]() mol��
mol��
���ֻ������Ӧ�ڣ�����c g CO2���壬��CuO�����ʵ���Ϊ��![]() ��
��
���ԣ�n��ȡֵ��ΧΪ��![]() mol��n��
mol��n��![]() mol��
mol��
��:(1)6.0 (2)C ![]()
(3) ![]() mol��n��
mol��n��![]() mol
mol

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�


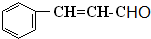



 ����һ�֣�
����һ�֣�
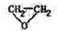
 ����
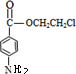
����
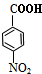 +HOCH2CH2Cl
+HOCH2CH2Cl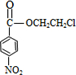 +H2O
+H2O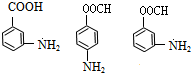

 )��
)��