题目内容
13.在一次实验中,学生需要使用1.0mol•L-1的NaOH溶液460mL,在实验室配制溶液时回答下列问题:(1)使用托盘天平称取NaOH固体20.0g;
(2)误差分析:用字母填写A、偏大 B、偏小 C、无影响
Ⅰ、溶解后溶液未冷却至室温,就转移到容量瓶中,立即定容,则浓度偏高;
Ⅱ、容量瓶中有少量蒸馏水,未干燥,则浓度无影响;
Ⅲ、定容时俯视液面,则浓度偏高.
分析 (1)实验室没有460mL容量瓶,但有500mL容量瓶,所以必须配置500mL溶液,则需要m(NaOH)=cVM=1.0mol/L×0.5L×40g/mol;
(2)根据c=$\frac{n}{V}$知,如果n偏小或V偏大则配制溶液浓度偏大,如果n偏大或V偏小,则配制溶液浓度偏高.
解答 解:(1)实验室没有460mL容量瓶,但有500mL容量瓶,所以必须配置500mL溶液,则需要m(NaOH)=cVM=1.0mol/L×0.5L×40g/mol=20.0g,故答案为:20.0;
(2)根据c=$\frac{n}{V}$知,如果n偏小或V偏大则配制溶液浓度偏大,如果n偏大或V偏小,则配制溶液浓度偏高,
Ⅰ、溶解后溶液未冷却至室温,就转移到容量瓶中,立即定容,溶液体积偏小,则浓度偏高,故答案为:偏高;
Ⅱ、容量瓶中有少量蒸馏水,未干燥,溶质物质的量及溶液体积都不变,则浓度无影响,故答案为:无影响;
Ⅲ、定容时俯视液面,配制溶液体积偏小,则浓度偏高,故答案为:偏高.
点评 本题考查一定物质的量浓度溶液配制,注意c=$\frac{n}{V}$中V指溶液体积而不是溶剂体积,易错点是容量瓶的选取,选取的容量瓶规格要等于或稍微大于配制溶液体积,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
3.下列物质中,原子间全部是通过共价键形成的是( )
| A. | NaOH | B. | NaCl | C. | H2SO4 | D. | (NH4)2SO4 |
4.下列说法不正确的是( )
| A. | 金刚石、氮化硼、碳化硅、石英、晶体硅、锗、刚玉均为原子晶体 | |
| B. | 干冰晶体、C60晶体、冰晶体、铜晶体中一个分子或金属原子周围有12个紧邻的分子或金属原子 | |
| C. | 面心立方最密堆积按ABABAB…的方式堆积,配位数为12,空间利用率为74% | |
| D. | 焰色反应的实质是发射光谱 | |
| E. | 第二主族金属元素的碳酸盐受热分解温度会越来越高,原因是晶格能越来越大. |
1.已知含氧酸可用通式XOm(OH)n表示,一般而言,该式中m 大的是强酸,m小的是弱酸.下列各含氧酸中酸性最强的是( )
| A. | H2CrO4 | B. | H3PO4 | C. | H3AsO4 | D. | HBrO4 |
7.用苯酚做下列实验,能成功的是( )
| A. | 与浓硫酸和浓硝酸混合液发生硝化反应 | |
| B. | 与乙醇发生酯化反应 | |
| C. | 在80℃的水中形成乳浊液 | |
| D. | 与福尔马林在沸水浴中便可发生缩聚反应制酚醛树脂 |
8.含有等物质的量的CH3COOH和CH3COONa的混合溶液中,下列说法正确的是( )
| A. | c(CH3COOH)+c(H+ )<c(OH-)+c(CH3COO-) | B. | c(H+ )+c(CH3COOH)=c(OH-)+c(CH3COO-) | ||
| C. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | D. | c(Na+)=c(CH3COOH)+c(CH3COO-) |
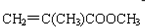 )旧法合成的反应是:
)旧法合成的反应是: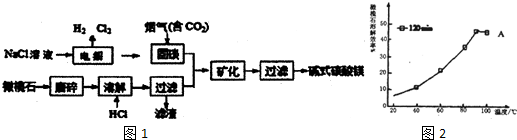
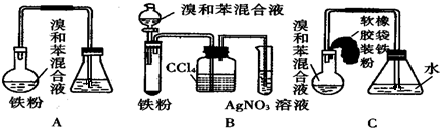
 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$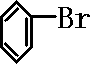 +HBr;装置A中左侧长导管的作用是导气和冷凝回流;装置A和C中的两处明显错误是锥形瓶未与大气相通、导管插入AgNO3(或水)溶液中.
+HBr;装置A中左侧长导管的作用是导气和冷凝回流;装置A和C中的两处明显错误是锥形瓶未与大气相通、导管插入AgNO3(或水)溶液中.