题目内容
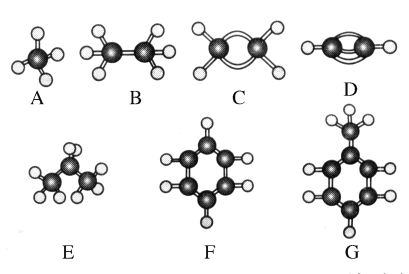
【题目】A~G是几种烃的分子球棍模型,据此回答下列问题:
(1)常温下含碳量最高的气态烃是________(填对应字母);
(2)能够发生加成反应的烃有________种;
(3)G的一氯代物有________种;E的二氯代物有_________种;
(4)写出C与溴的四氯化碳溶液反应的化学方程式______________________;
(5)写出F与浓硝酸和浓硫酸反应的化学方程式________________________。反应类型为_______
现有上面A、B、C三种有机化合物:(以下均用结构简式作答)
(6)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是_____。
(7)等质量的以上三种物质燃烧时,生成二氧化碳最多的是__________,生成水最多的是__________。
(8)在120℃、1.01×105Pa时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是__________。
【答案】D 4 4 4 CH2=CH2+Br2→CH2Br-CH2Br ![]() 取代反应 CH3CH3 CH2=CH2 CH4 CH4、CH2=CH2
取代反应 CH3CH3 CH2=CH2 CH4 CH4、CH2=CH2
【解析】
根据结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,然后再根据各有机物分子的组成、结构和性质进行解答该题。
由图示有机物的球棍模型可知:A为甲烷、B为乙烷、C为乙烯、D为乙炔、E为丙烷、F为苯、G为甲苯。
(1)常温下含碳量最高的气态烃是为乙炔,故合理选项是D;
(2)能够发生加成的烃有乙烯、乙炔、苯和甲苯4种物质,所以答案为:4种;
(3)G是甲苯,甲苯的一卤代物有甲基上、苯环的甲基的邻位、间位、对位四种不同的确定产物,所以有4种;E是丙烷,其二氯代物有1,1-二氯丙烷、2,2-二氯丙烷、1,2-二氯丙烷、1,3-二氯丙烷4种二氯取代产物;
(4) C是乙烯,C与溴的四氯化碳溶液发生加成反应产生1,2-二溴乙烷,反应的化学方程式为CH2=CH2+Br2→CH2Br-CH2Br;
(5)F为苯,苯可与浓硝酸在浓硫酸作用下加热50~60℃发生取代反应,产生硝基苯和水,反应的方程式为:![]() ;
;
(6)根据n=![]() 可知:同状况、同体积的甲烷、乙烷、乙烯的体积比等于它们的物质的量的比,1molCH4完全燃烧消耗2molO2,1molCH3CH3完全燃烧消耗3.5molO2,1molCH2=CH2完全燃烧消耗3molO2,可见三种物质完全燃烧时耗去O2的量最多的是乙烷,结构简式为CH3CH3。
可知:同状况、同体积的甲烷、乙烷、乙烯的体积比等于它们的物质的量的比,1molCH4完全燃烧消耗2molO2,1molCH3CH3完全燃烧消耗3.5molO2,1molCH2=CH2完全燃烧消耗3molO2,可见三种物质完全燃烧时耗去O2的量最多的是乙烷,结构简式为CH3CH3。
(7)CH4、CH3CH3、CH2=CH2三种物质中C、H原子个数比为1:4、1:3、1:2,可见等质量的上述三种物质中,含碳量最大的是乙烯,含氢量最大的是甲烷。等质量的以上三种物质燃烧时,C元素含量越多,燃烧生成二氧化碳最多,含氢量越大,燃烧产生的水最多,因此在上述三种物质中等质量燃烧产生的CO2最多的是CH2=CH2,生成水最多的是甲烷CH4。
(8)在120℃、1.01×105Pa时,水为气态,假设混合烃平均化学式为CxHy,根据烃燃烧的方程式:CxHy+(x+![]() )O2
)O2![]() xCO2+
xCO2+![]() H2O,若有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,则1+(x+
H2O,若有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,则1+(x+![]() )=x+
)=x+![]() ,y=4,在上述物质中,分子中H原子数等于4的有甲烷CH4、乙烯CH2=CH2,因此这两种气体是CH4、CH2=CH2。
,y=4,在上述物质中,分子中H原子数等于4的有甲烷CH4、乙烯CH2=CH2,因此这两种气体是CH4、CH2=CH2。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
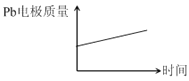
同步拓展阅读系列答案【题目】为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O![]() Al2O3+3H2↑
Al2O3+3H2↑
电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:2Al+3H2O-6e-=Al2O3+6H+ |
D |
|
|
A. AB. BC. CD. D