题目内容
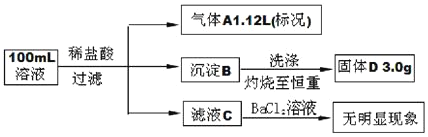
【题目】以磷石膏![]() 主要成分CaSO4,杂质SiO2、Al2O3等
主要成分CaSO4,杂质SiO2、Al2O3等![]() 为原料可制备轻质CaCO3。
为原料可制备轻质CaCO3。

“转化”步骤中浆料清液的pH和c(SO42-)随时间变化如图,下列说法正确的是

A.为提高磷石膏粉的转化率,应通入过量的CO2
B.“转化”步骤,应控制溶液的pH约为7
C.高温煅烧时可发生反应![]() ,从而除去SiO2杂质
,从而除去SiO2杂质
D.向浸取液中通入CO2,可沉淀出几乎所有钙元素,后经过滤、洗涤、烘干即可获得轻质CaCO3
【答案】C
【解析】
磷石膏氨水的浆料中通入CO2可生成碳酸盐或碳酸氢盐,过滤后滤液为硫酸铵、氨水,滤渣为CaCO3、SiO2、Al2O3等,高温煅烧可生成CaSiO3、Ca(AlO2)2等,加入氯化铵溶液充分浸取,可生成H2SiO3、Al(OH)3、CaCl2,最终可生成CaCO3,据此进行分析和判断。
A. 为提高磷石膏粉的转化率,可利用搅拌、增大氨水浓度等方法,通入过量的CO2不能提高磷石膏粉的转化率,A项错误;
B. “转化”时,发生的是硫酸钙转化为碳酸钙的反应,当控制pH<8时,CaCO3逐渐溶解,溶液中Ca2+浓度增大,形成了CaSO4的饱和溶液,因此“转化”步骤,不能将溶液的pH控制为7,B项错误;
C. 高温煅烧时,碳酸钙可与SiO2反应生成硅酸钙与CO2,可达到除去SiO2的目的,且方程式为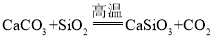 ,C项正确;
,C项正确;
D. 向浸取液中通入CO2,可沉淀Ca2+,但当通入过量的CO2时,CaCO3逐渐溶解,因此通入CO2不能沉淀出所有钙元素,D项错误;
答案选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是
选项 | 反应类型 | 反应条件 |
A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D