题目内容
【题目】写出下列反应的离子方程式或化学方程式.
(1)用稀硫酸清除铁锈(Fe2O3)(写出离子方程式):
(2)FeCl3溶液中加入NaOH溶液(写出离子方程式):
(3)盐酸跟碳酸氢钠溶液反应(写出离子方程式):
(4)少量CO2通入澄清石灰水中(写出离子方程式): .
(5)Cu2++2OH﹣=Cu(OH)2↓(写出化学方程式) .
【答案】
(1)Fe2O3+6H+=2Fe3++3H2O
(2)Fe3++3OH﹣═Fe(OH)3↓
(3)H++HCO ![]() =CO2↑+H2O
=CO2↑+H2O
(4)CO2+Ca2++2OH﹣═CaCO3↓+H2O
(5)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
【解析】解:(1)用稀硫酸清除铁锈(Fe2O3),离子方程式:Fe2O3+6H+=2Fe3++3H2O;所以答案是:Fe2O3+6H+=2Fe3++3H2O;(2)FeCl3溶液中加入NaOH溶液,反应的离子方程式:Fe3++3OH﹣═Fe(OH)3↓;所以答案是:Fe3++3OH﹣═Fe(OH)3↓;(3)盐酸与碳酸氢钠反应生成氯化钠、水和二氧化碳,离子方程式:H++HCO ![]() =CO2↑+H2O;所以答案是:H++HCO3﹣=CO2↑+H2O;(4)少量CO2通入澄清石灰水中,反应生成碳酸钙和水,离子方程式:CO2+Ca2++2OH﹣═CaCO3↓+H2O;所以答案是:CO2+Ca2++2OH﹣═CaCO3↓+H2O;(5)Cu2++2OH﹣=Cu(OH)2↓表示可溶性铜盐与强碱反应生成氢氧化铜沉淀和可溶性盐,可以表示硫酸铜与氢氧化钠反应的离子方程式,该反应化学方程式为:Cu SO4+2NaOH=Cu(OH)2↓+Na2SO4;所以答案是:Cu SO4+2NaOH=Cu(OH)2↓+Na2SO4 .
=CO2↑+H2O;所以答案是:H++HCO3﹣=CO2↑+H2O;(4)少量CO2通入澄清石灰水中,反应生成碳酸钙和水,离子方程式:CO2+Ca2++2OH﹣═CaCO3↓+H2O;所以答案是:CO2+Ca2++2OH﹣═CaCO3↓+H2O;(5)Cu2++2OH﹣=Cu(OH)2↓表示可溶性铜盐与强碱反应生成氢氧化铜沉淀和可溶性盐,可以表示硫酸铜与氢氧化钠反应的离子方程式,该反应化学方程式为:Cu SO4+2NaOH=Cu(OH)2↓+Na2SO4;所以答案是:Cu SO4+2NaOH=Cu(OH)2↓+Na2SO4 .

 小学课时特训系列答案
小学课时特训系列答案【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下: 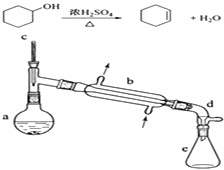
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是 .
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是 .
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有 ABE (填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验所得到的环己烯产率是 . (保留两位有效数字)
(注:产率= ![]() ×100%)
×100%)