题目内容
13.已知NaHSO3溶液呈弱酸性.在0.1mol•L-1NaHSO3溶液中,下列关系正确的是( )| A. | c(Na+)+c(H+)=c(HSO3-)+c(OH-)+c(SO32-) | B. | c(HSO3-)+c(SO32-)=0.1mol•L-1 | ||
| C. | c(SO32-)<c(H2SO3) | D. | c(Na+)=c(H2SO3)+c(HSO3-)+c(SO32-) |
分析 H2SO3是二元弱酸,NaHSO3溶液呈酸性,说明亚硫酸氢根离子水解程度小于电离程度,然后根据物料守恒和电荷守恒来分析解答.
解答 解:H2SO3是二元弱酸,NaHSO3溶液呈酸性,说明亚硫酸氢根离子水解程度小于电离程度,
A.亚硫酸氢钠溶液呈电中性,溶液中存在电荷守恒,所以c(Na+)+c(H+)=c(HSO3-)+c (OH-)+2c(SO32-),故A错误;
B.亚硫酸氢钠溶液中存在物料守恒,即c(Na+)=c(HSO3-)+c(SO32-)+c(H2SO3)=0.1mol/L,故c(HSO3-)+c(SO32-)<0.1mol/L,故B错误;
C.NaHSO3溶液中亚硫酸氢根离子无论电离还是水解都是较微弱的,所以溶液中还是以HSO3-存在为主,NaHSO3溶液呈酸性,说明亚硫酸氢根离子水解程度小于电离程度,所以c(SO32-)>c(H2SO3),故C错误;
D.亚硫酸氢钠溶液中存在物料守恒,即c(Na+)=c(HSO3-)+c(SO32-)+c(H2SO3),故D正确;
故选D.
点评 本题考查弱电解质和盐类水解问题,题目难度中等,注意根据溶液电中性和物料守恒解答该题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.氮的固定主要有三大途径,它们是生物固氮、大气固氮、工业固氮;氮肥主要有铵态氮肥、硝态氮肥和有机氮肥,目前氮肥中使用量最多的一种肥料是尿素;含氮、磷、钾三要素中的两种或两种以上的化学肥料称复合肥料.
4.分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法.下列关于“Na2SiO3”的分类不正确的是( )
| A. | 电解质 | B. | 弱酸盐 | C. | 强碱盐 | D. | 碱性氧化物 |
1.据湖北电视台2000年3月6日报道,汉江流域发生第三次“水华”现象,江面上有大量的白色漂浮物,类似于海面上“红潮”,取水样分析:绿藻含量比正常情况下偏高很多,含O2量明显偏低,浑浊度增加.造成汉江“水华”现象最可能的原因是( )
| A. | 水土流失 | |
| B. | 汉江流域农业生产中长期使用农药 | |
| C. | 生活废水大量排入汉江,使水质富营养化 | |
| D. | 有毒的废水大量排入汉江 |
8.下列关于能量变化的说法正确的是( )
| A. | 相同质量的水和冰相比较,冰的能量高 | |
| B. | 化学反应过程中能量的变化只有吸热和放热两种表现形式 | |
| C. | 化学反应既遵循质量守恒,也遵循能量守恒 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
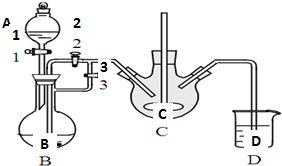 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得: