题目内容
已知25 ℃、101 kPa条件下:4Al(s)+3O2(g)====2Al2O3(s);ΔH=-2834.9 kJ·mol-1
4Al(s)+2O3(g) ====2Al2O3(s);ΔH=-3119.1 kJ·mol-1
由此得出的正确结论是
A.等质量的O2比O3能量低,由O2变O3为吸热反应
B.等质量的O2比O3能量低,由O2变O3为放热反应
C.O3比O2稳定,由O2变O3为吸热反应
D.O2比O3稳定,由O2变O3为放热反应
A
解析:生成相同Al2O3(s)放热越少,代表反应物能量越低,所以A正确。

练习册系列答案
相关题目
下列有关热化学方程式的评价合理的是( )
|
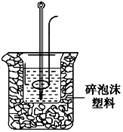
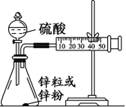
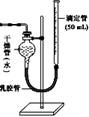
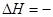 393.51
kJ/mol①;C(金刚石) + O2(g) ==== CO2(g)
393.51
kJ/mol①;C(金刚石) + O2(g) ==== CO2(g)