题目内容
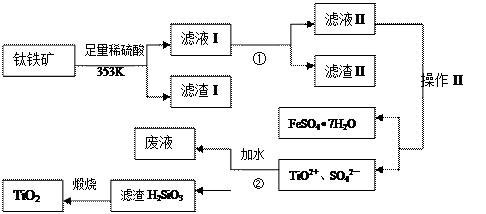
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3 MgO、CaO等,生产工艺流程示意如下:
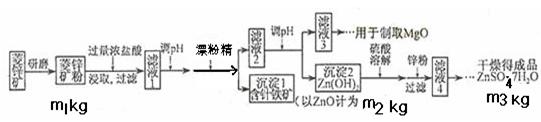
(1)将菱锌矿研磨成粉的目的是____ _,滤液1后两步操作的目是: 。
(2)完成加漂粉精反应的离子方程式:
□Fe(OH)2+□____+□_____ →□Fe(OH)3+□Cl-
(3)针铁矿的组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)为了了解如何调节滤液2的PH,请写出两个你认为需要查阅的数据
, (用文字叙述)
(5) “滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________。

(1)将菱锌矿研磨成粉的目的是____ _,滤液1后两步操作的目是: 。
(2)完成加漂粉精反应的离子方程式:
□Fe(OH)2+□____+□_____ →□Fe(OH)3+□Cl-
(3)针铁矿的组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)为了了解如何调节滤液2的PH,请写出两个你认为需要查阅的数据
, (用文字叙述)
(5) “滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________。
(共12分,每小题2分)1)增大反应物接触面积或增大反应速率或使反应更充分,除去含铁杂质。
(2)2Fe(OH)2+ClO-+H2O →2Fe(OH)3+Cl-
(3)FeO(OH)(或其它合理答案)
(4)Mg(OH)2开始沉淀时的pH、Zn(OH)2开始沉淀时的pH, Mg(OH)2沉淀完全时的pH、Zn(OH)2沉淀完全时的pH(任写两个即可)
(5)蒸发浓缩、冷却结晶(或其它合理答案)
(6)125m2/81m1(或其它合理答案)
(2)2Fe(OH)2+ClO-+H2O →2Fe(OH)3+Cl-
(3)FeO(OH)(或其它合理答案)
(4)Mg(OH)2开始沉淀时的pH、Zn(OH)2开始沉淀时的pH, Mg(OH)2沉淀完全时的pH、Zn(OH)2沉淀完全时的pH(任写两个即可)
(5)蒸发浓缩、冷却结晶(或其它合理答案)
(6)125m2/81m1(或其它合理答案)
略

练习册系列答案
相关题目
 生的反应为:
生的反应为: 92),则产品中硫酸亚铁铵晶体纯度的计算式可表达为:w%= 。
92),则产品中硫酸亚铁铵晶体纯度的计算式可表达为:w%= 。
 成。已知常温下,Al(OH)3浊液的pH=3,其Ksp=1×10-36,则其中c(Al3+)= ▲ 。
成。已知常温下,Al(OH)3浊液的pH=3,其Ksp=1×10-36,则其中c(Al3+)= ▲ 。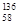 Ce、
Ce、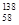 Ce、
Ce、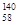 Ce、
Ce、 Ce,它们互为同素异形体
Ce,它们互为同素异形体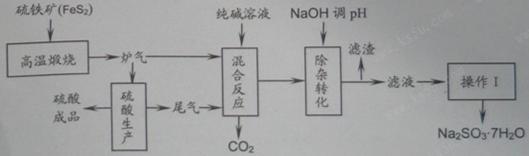
 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________