题目内容
20.溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作.工业以浓缩海水为原料提取溴的部分过程如下:
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

①A装置中通入a气体的目的是(用离子方程式表示)Cl2+2Br-=2Cl-+Br2;
②A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是吹出Br2;
③B装置中通入的b气体是SO2,目的是使溴蒸气转化为氢溴酸以达到富集的目的,试写出该反应的化学方程式Br2+SO2+2H2O=2HBr+H2SO4;
④C装置的作用是吸收未反应的Cl2、Br2和SO2.
分析 由流程可知,氯气与浓缩海水中溴离子发生氧化还原反应生成溴,在吹出塔中富集溴,然后在吸收塔中溴、二氧化硫和水发生氧化还原反应生成硫酸和HBr;
由实验装置可知,a为氯气,可氧化溴离子,热空气可将生成的溴蒸气吹出,气体b为二氧化硫,在B装置中发生氧化还原反应生成硫酸和HBr,C装置为尾气处理装置,吸收氯气、二氧化硫、溴等,以此来解答.
解答 解:①要想使溴离子变成溴单质,则加入的a能和溴离子发生反应生成溴单质,氯气能和溴离子发生置换反应生成溴单质,离子反应方程式为Cl2+2Br-=2Cl-+Br2,
故答案为:Cl2+2Br-=2Cl-+Br2;
②溴易挥发,升高温度促进其挥发,所以通入热空气的目的是吹出Br2,故答案为:吹出Br2;
③使溴蒸气转化为氢溴酸以达到富集的目的,可知气体b为SO2,发生的反应为Br2+SO2+2H2O=2HBr+H2SO4,
故答案为:SO2;Br2+SO2+2H2O=2HBr+H2SO4;
④氯气不可能完全反应,氯气和溴离子反应生成溴单质,未反应的二氧化硫、氯气和溴都有毒,不能直接排空,且这几种物质都能和碱反应,所以C装置是尾气处理装置,可知C的作用为吸收未反应的Cl2、Br2和SO2,
故答案为:吸收未反应的Cl2、Br2和SO2.
点评 本题考查海水资源开发利用及海水提溴,为高频考点,涉及氧化还原反应、离子反应及流程分析,注重基础知识的综合运用,侧重分析与应用能力的考查,题目难度中等.

练习册系列答案
相关题目
10.天然纤维是自然界原有的或经人工培植的植物上、人工饲养的动物上直接取得的纺织纤维.化学纤维指用天然的或合成的聚合物为原料,经化学方法制成的纤维.下列物质属于天然纤维且其主要成份是纤维素的是( )
| A. | 光导纤维 | B. | 人造丝 | C. | 棉花 | D. | 蚕丝 |
11.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的元素的原子最外层电子数之和为20.则下列说法不正确的是( )
| X | Y | |||
| W | Z |
| A. | 最高价氧化物的水化物的酸性:X<Z | |
| B. | 原子半径大小:Y<W | |
| C. | 工业上用电解熔融的W与Z所形成的化合物来制取W | |
| D. | W和Y形成的化合物可与Z的氢化物的水溶液发生反应 |
8.在实验室中从苯酚中分离出苯,可选用下列装置中的( )
| A. | 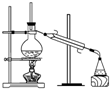 | B. |  | C. | 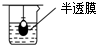 | D. | 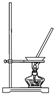 |
15.哈伯因发明用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下使该反应发生N2+3H2?2NH3.下列说法正确的是( )
| A. | 达到化学平衡时,N2完全转化为NH3 | |
| B. | 一定条件下达到化学平衡时,N2、H2和NH3的物质的量浓度之比为1:3:2 | |
| C. | 单位时间内消耗a mol N2同时消耗2amol NH3,说明该反应已达到平衡状态 | |
| D. | 达到化学平衡时,正反应和逆反应速率相等,且都为零 |
5.下列化学式所表示的化合物中,具有两种或两种以上同分异构体的有( )
| A. | CH2O2 | B. | CH2Cl2 | C. | C7H8O | D. | C2H5NO2 |
12.为了除去下列各组混合物中括号内的物质,所选用的试剂与主要分离方法都正确的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 浓溴水 | 过滤 |
| B | 碘水(水) | 花生油 | 萃取 |
| C | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| D | 鸡蛋清溶液(氯化钠溶液) | 蒸馏水 | 渗析 |
| A. | A | B. | B | C. | C | D. | D |
9.工业上由氯气与消石灰反应制备漂粉精,其化学式可以用xCa(ClO)2•yCaCl2•zCa(OH)2(x、y、z为简单整数)来表示.某兴趣小组同学对漂粉精进行定性、定量探究如下:
Ⅰ.证明漂粉精中含有CaCl2
①向漂粉精固体中滴加足量浓硫酸,观察到黄绿色气体生成.写出生成黄绿色气体的化学反应方程式:Ca(ClO)2+CaCl2+4H2SO4(浓)=2Ca(HSO4)2+2Cl2↑+2H2O
(或Ca(ClO)2+CaCl2+2H2SO4(浓)=CaSO4+2Cl2↑+2H2O).
②将生成的黄绿色气体缓缓通过足量碱石灰,碱石灰增重,并收集到无色气体.推测生成气体中除Cl2,还含有HCl、O2(填化学式).
Ⅱ.证明漂粉精中含有Ca(OH)2[已知电离常数:Ka1(H2CO3)>Ka(HClO)>Ka2(H2CO3)]
①将少量漂粉精溶于水后,测定其pH值为12.3.采用的测定方法可能是c(选填答案编号).
a.使用广泛pH试纸 b.使用精密pH试纸c.使用pH计 d.以酚酞为指示剂进行酸碱中和滴定
②下列探究步骤的设计中,对证明该结论无意义的是a(选填答案编号).
a.向漂粉精溶液中通入适量CO2,测定溶液的pH值变化
b.向漂粉精溶液中加入适量碳酸氢钠固体,测定溶液pH值变化
c.向漂粉精溶液中加入适量亚硫酸钠固体,测定溶液pH值变化 ③
Ⅲ.测定漂粉精中有效成分的含量
【实验原理】ClO-+2I-+2H+=Cl-+I2+H2O; I2+2S2O32-=2I-+S4O62-
【实验步骤】
i.称取7.740g漂粉精固体,溶解,配成250mL溶液;
ii.量取该溶液5.00mL于锥形瓶,加入过量KI溶液、酸化,并加入指示剂;
iii.用0.100mol/L Na2S2O3标准溶液滴定至终点,记录始末读数;
iv.重复ii、iii操作,记录始末读数.
①该实验中要使用的定量仪器除电子天平外还有滴定管、250mL容量瓶(写名称).
②步骤ii中加入的指示剂为淀粉(写名称),当观察到溶液由蓝色变为无色,且半分钟内不变化
时,达到滴定终点.
③实验数据如下:
若理论上滴定时消耗标准溶液27.00mL,则相对误差为-0.185%(保留3位有效数字).
④该漂粉精中Ca(ClO)2的质量分数为(以理论值计)0.624(保留3位有效数字).
Ⅰ.证明漂粉精中含有CaCl2
①向漂粉精固体中滴加足量浓硫酸,观察到黄绿色气体生成.写出生成黄绿色气体的化学反应方程式:Ca(ClO)2+CaCl2+4H2SO4(浓)=2Ca(HSO4)2+2Cl2↑+2H2O
(或Ca(ClO)2+CaCl2+2H2SO4(浓)=CaSO4+2Cl2↑+2H2O).
②将生成的黄绿色气体缓缓通过足量碱石灰,碱石灰增重,并收集到无色气体.推测生成气体中除Cl2,还含有HCl、O2(填化学式).
Ⅱ.证明漂粉精中含有Ca(OH)2[已知电离常数:Ka1(H2CO3)>Ka(HClO)>Ka2(H2CO3)]
①将少量漂粉精溶于水后,测定其pH值为12.3.采用的测定方法可能是c(选填答案编号).
a.使用广泛pH试纸 b.使用精密pH试纸c.使用pH计 d.以酚酞为指示剂进行酸碱中和滴定
②下列探究步骤的设计中,对证明该结论无意义的是a(选填答案编号).
a.向漂粉精溶液中通入适量CO2,测定溶液的pH值变化
b.向漂粉精溶液中加入适量碳酸氢钠固体,测定溶液pH值变化
c.向漂粉精溶液中加入适量亚硫酸钠固体,测定溶液pH值变化 ③
Ⅲ.测定漂粉精中有效成分的含量
【实验原理】ClO-+2I-+2H+=Cl-+I2+H2O; I2+2S2O32-=2I-+S4O62-
【实验步骤】
i.称取7.740g漂粉精固体,溶解,配成250mL溶液;
ii.量取该溶液5.00mL于锥形瓶,加入过量KI溶液、酸化,并加入指示剂;
iii.用0.100mol/L Na2S2O3标准溶液滴定至终点,记录始末读数;
iv.重复ii、iii操作,记录始末读数.
①该实验中要使用的定量仪器除电子天平外还有滴定管、250mL容量瓶(写名称).
②步骤ii中加入的指示剂为淀粉(写名称),当观察到溶液由蓝色变为无色,且半分钟内不变化
时,达到滴定终点.
③实验数据如下:
| 实验编号 | 1 | 2 | 3 |
| 消耗Na2S2O3体积/mL | 26.90 | 27.00 | 26.95 |
④该漂粉精中Ca(ClO)2的质量分数为(以理论值计)0.624(保留3位有效数字).
10.生活中金属的使用已成为一种日常,在生活中使用的金属中,除少量极不活泼金属外几乎所有的金属都以化合态存在,那么我们的问题来了,请问下列各种冶炼方法中,可制得相应金属的是( )
| A. | 加热氧化银 | B. | 煅烧碳酸钙 | ||
| C. | 电解氯化钠溶液 | D. | 氯化镁与铝粉高温共热 |