题目内容
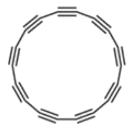
【题目】如图所示是某些晶体的结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一部分。
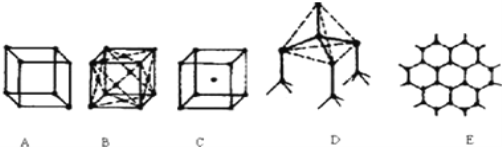
(1)其中代表金刚石的是(填编号字母,下同)____。
(2)其中代表石墨的是____。
(3)其中代表NaCl的是___。
(4)代表CsCl的是___。
(5)代表干冰的是____。
【答案】D E A C B
【解析】
(1) 在金刚石晶胞中,每个碳可与周围四个碳原子形成共价键,将这四个碳原子连结起来后可以形成正四面体,体心有一个碳原子,所以图D为金刚石,故答案为:D;
(2) 石墨是层状结构,在层与层之间以范德华力相互作用,有分子晶体的特点,在层内碳与碳以共价键相互作用,形成六边形,所以图E为石墨的结构,故答案为:E;
(3) 氯化钠是离子晶体,其构成微粒是阴阳离子,NaCl晶胞是简单的立方单元,所以图A为氯化钠结构,故答案为:A;
(4) 氯化铯也是离子晶体,阴阳离子的配位数均是8,即每个铯离子与8个氯离子紧邻,所以C图为氯化铯的结构,故答案为:C;
(5) 干冰是分子晶体,CO2分子位于立方体的顶点和面心上,以顶点上的CO2分子为例,与它距离最近的CO2分子分布在与该顶点相连的12个面的面心上,所以图B为干冰晶体,故答案为:B。

【题目】某实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素。设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
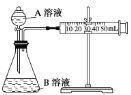
(1)通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小。实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见下表:
序号 | A溶液 | B溶液 |
① | 2mL0.1mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液 |
② | 2mL0.2mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液 |
③ | 2mL0.2mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液和少量MnSO4 |
该实验探究的是___对化学反应速率的影响。在反应停止之前,相同时间内针管中所得CO2的体积由大到小的顺序是___(用实验序号填空)。
(2)某组同学利用如图完成该实验。请分析导管a的两点作用:①___;②___。