题目内容
18.一定条件下用甲烷可以消除氮氧化物(NOx)的污染.已知:①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1 160kJ•mol-1
下列叙述正确的是( )
| A. | CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(l)△H=-867 kJ•mol-1 | |
| B. | CH4催化还原NOx为N2的过程中,若x=1.6,则转移电子3.2 mol | |
| C. | 若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ | |
| D. | 若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移电子3.2 mol |
分析 A.由反应①+②可得到2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O( g ),再利用化学计量数与反应热成正比来计算;
B.x=1.6,1molNOx中NO2、NO分别为0.6mol、0.4mol,转移的电子数为0.6mol×(4-0)+0.4mol×(2-0);
C.利用热化学反应方程式中化学计量数与反应热的关系来计算;
D.利用n=$\frac{V}{{V}_{m}}$计算甲烷的物质的量,再利用碳元素化合价的变化来计算转移的电子数.
解答 解:A.反应①+②可得到2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O( g ),△H=(-574kJ•mol-1)+(-1160kJ•mol-1)=-1734kJ•mol-1,
则CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O( g )△H=-867kJ•mol-1,若生成液态水,则放出的热量大于867KJ,故A错误;
B.x=1.6,1molNOx中NO2、NO分别为0.6mol、0.4mol,转移的电子数为0.6mol×(4-0)+0.4mol×(2-0)=3.2mol,但该反应中NOx的物质的量不确定,则转移的电子数不确定,故B错误;
C.由CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O( g )△H=-867kJ•mol-1,放出的热量为0.2mol×867kJ•mol-1=173.4kJ,故C正确;
D.甲烷的物质的量为$\frac{4.48L}{22.4L/mol}$=0.2mol,碳元素的化合价由-4价升高为+4价,则转移的电子总数为为0.2mol×8=1.6mol,故D错误;
故选C.
点评 本题考查学生利用盖斯定律来计算反应的反应热,并学会利用化学计量数与反应热的关系、利用化合价的变化分析电子转移的数目来就解答即可.

| A. | Al2(SO4)3═2Al3++3SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | Ba(OH)2═Ba2++2OH- | D. | Na2SO4═2Na++SO42- |
| A. | 25mL 0.1mol•L-1的BaCl2溶液 | B. | 50mL 0.3mol•L-1的NaCl溶液 | ||
| C. | 50 mL0.3mol•L-1的FeCl3溶液 | D. | 75 mL 0.1mol•L-1的KCl溶液 |
| A. | 12C和14C | B. | 金刚石与石墨 | ||
| C. | CH3CHO与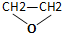 | D. | CH3CHCH2CH3与CH3CH2CH2CHCH3 |
(1)如图1所示,选取必要的实验装置,正确的连接顺序为CAB(填序号)
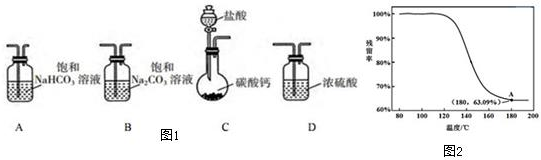
(2)为确定制得的固体样品是纯净的NaHCO3 小组同学提出下列实验方案:
甲方案:将样品溶液与饱和澄清石灰水反应,观察现象.
乙方案:将样品溶液与BaCl2 观察现象.
丙方案:测定pH法
丁方案:热重分析法
①判定甲方案不可行(填“可行”或“不可行”)
②为判定乙方案的可行性,某同学用分析纯净的NaHCO3配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下:
| NaHCO3溶液 BaCl2浓度 | 0.2mol•L-1 | 0.1mol•L-1 | 0.02mol•L-1 |
| 0.2mol•L-1 | 浑浊 | 浑浊 | 少许浑浊 |
| 0.1mol•L-1 | 浑浊 | 少许浑池 | 无现籴 |
| 0.02mol•L-1 | 少许浑油 | 尤现象 | 尤现象 |
[已知:0.1 mol•L-1NaHC03溶液电离出的c(CO32-)为0.0011mol•L-1,Ksp(BaCO3)=5.1×10-9]
答:Qc=c(Ba2+)×c(CO32-)=$\frac{0.2}{2}$×0.0011=1.1×10-4>5.1×10-9.
(Ⅱ)产生浑浊的离子方程式为Ba2++2HCO3-=BaCO3↓+CO2↑+H2O.
③使用pH计进行测定的丙方案如下:
取m克的固体样品溶解于水配成Vml的溶液,用pH计测pH:
还应补充的实验是:另取等质量的分析纯NaHC03溶于水中配成V mL的溶液,用pH计测pH
④进行丁方案实验,得到固体残留率随温度变化的曲线如图2所示,根据A点坐标得到的结论是制得的固体样品是纯净的NaHCO3.
(残留率=$\frac{剩余固体的质量}{原始固体的质量}×100%$)
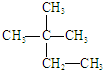 ③氧气 ④氯气 ⑤
③氧气 ④氯气 ⑤ ⑥${\;}_{17}^{37}$Cl ⑦${\;}_{17}^{35}$Cl ⑧臭氧.
⑥${\;}_{17}^{37}$Cl ⑦${\;}_{17}^{35}$Cl ⑧臭氧.