题目内容
【题目】[物质结构与性质]
[Zn(CN)4]2﹣在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2﹣+4H++4H2O═[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为 .
(2)1molHCHO分子中含有σ键的数目为mol.
(3)HOCH2CN分子中碳原子轨道的杂化轨道类型是 .
(4)与H2O分子互为等电子体的阴离子为 .
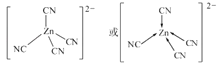
(5)[Zn(CN)4]2﹣中Zn2+与CN﹣的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2﹣的结构可用示意图表示为 .
【答案】
(1)1s22s22p63s23p63d10或[Ar]3d10
(2)3
(3)sp3杂化、sp杂化
(4)NH2﹣
(5)
【解析】(1)Zn是30号元素,其原子核外有30个电子,失去最外层两个电子生成锌离子,根据构造原理书写其核外电子排布式为1s22s22p63s23p63d10或[Ar]3d10 , 所以答案是:1s22s22p63s23p63d10或[Ar]3d10 ;
(2)单键为σ键,双键含有1个σ键和1个π键,三键含有1个σ键和2个π键,HCHO分子中含有2个C﹣H键、1个C=O双键,分子中含有3个σ键,所以1mol甲醛(HCHO)分子中含有的σ键数目为3mol,所以答案是:3;
(3) 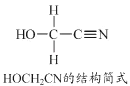 ,其中与羟基(﹣OH)相连的一个碳为饱和碳原子,价层电子对=4+0=4,杂化轨道类型为SP3 , 另外一碳原子与氮原子形成碳氮三键,三键含有1个σ键和2个π键,价层电子对=2+
,其中与羟基(﹣OH)相连的一个碳为饱和碳原子,价层电子对=4+0=4,杂化轨道类型为SP3 , 另外一碳原子与氮原子形成碳氮三键,三键含有1个σ键和2个π键,价层电子对=2+ ![]() =2,所以碳原子杂化轨道类型为SP,
=2,所以碳原子杂化轨道类型为SP,
所以答案是:sp3杂化、sp杂化;
(4)原子个数相等、价电子数相等的微粒为等电子体,与水互为等电子体的微粒该是3原子最外层电子数为8的分子或离子,这样的微粒有:H2S、NH2﹣ , 阴离子为:NH2﹣ , 所以答案是:NH2﹣;
(5)[Zn(CN)4]2﹣中锌离子提供空轨道,C原子提供电子对形成配位键,结构示意图表示为:  ,图示箭头表示碳提供电子给锌,所以答案是:
,图示箭头表示碳提供电子给锌,所以答案是:  .
.

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】在化学研究中,往往可以通过观察现象认识物质变化的情况.请分析以下一组有现象变化的化学反应.
实验 | 试剂及操作 | 现象 | |
试管 | 滴管 | ||
| 饱和Na2SlO3溶液(含2滴酚酞) | 先滴加1.0mL0.5molL﹣1NaOH溶液:再滴加1.5mL1.0molL﹣1H2SO4溶液 | Ⅰ.红色溶液中出现胶状沉淀 |
0.1molL﹣1AlCl3溶液 | Ⅱ.加碱时 ;加酸时产生白色沉淀,又逐渐溶解直至消失 | ||
0.1molL﹣1Fe(NO3)2溶液 | Ⅲ.加碱时 ;加酸后溶液变为黄色 | ||
新制饱和氯水 | Ⅳ.加碱时溶液变为无色;加酸后无色溶液变为浅黄绿色 | ||
(1)用离子方程式解释现象I中出现胶状沉淀的原因: .
(2)II中加碱时出现的现象是 , 此现象说明溶液中发生反应的离子方程式是 .
(3)III中加碱时出现的现象是 .
(4)用离子方程式解释IV中加碱时出现的现象 .
(5)滴加试剂顺序的变化,会影响溶液中的现象和发生的反应,请继续分析以下实验.
实验 | 试剂及操作 | 现象 | |
试管 | 滴管 | ||
| 0.1 molL﹣1 Fe(NO3)2溶液 | 先滴加1.5 mL 1.0 molL﹣1 H2SO4溶液; | V.加酸时溶液无明显现象;加碱后溶液依然没有明显变化 |
①探究加酸时Fe(NO3)2溶液中是否发生了反应:
向1.0mL 0.1molL﹣1Fe(NO3)2溶液中 , 溶液立即变红,说明溶液中含Fe3+ , 证明加酸时溶液中发生了反应.
②推测溶液中产生Fe3+的可能原因有两种:
a.酸性条件下,0.1molL﹣1 Fe(NO3)2溶液中的Fe2+被NO3﹣氧化;
b.(用离子方程式表示).

