题目内容
下列有关说法正确的是
| A.催化剂通过降低化学反应的焓变加快化学反应速率 |
| B.铅蓄电池充电时,标有“—”的电极应与电源的负极相连 |
| C.温度保持不变,向水中加入钠盐对水的电离一定没有影响 |
| D.向醋酸钠溶液中加水稀释时.溶液中所有离子浓度都减小 |
B
解析试题分析:A、催化剂通过降低化学反应的活化能加快化学反应速率,A不正确;
B、铅蓄电池充电时,标有“—”的电极应与电源的负极相连,标有“+”的电极应与电源的正极相连,B正确;
C、温度保持不变,向水中加入钠盐对水的电离不一定没有影响,例如加入硫酸氢钠抑制水的电离,C不正确;
D、向醋酸钠溶液中加水稀释,促进CH3COO-的水解,溶液的碱性降低,酸性增强,D不正确,答案选B。
考点:考查外界条件对反应速率、电离平衡、水解平衡的影响以及电化学原理的应用等

练习册系列答案
相关题目
一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应,在t1时达到平衡:
A(g)+ B(g) xC(g)+D(s)。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变
xC(g)+D(s)。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变
化如图所示。有关说法正确的是
| A.反应方程式中x=2 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量D |
| D.t1~t3间该反应的平衡常数相同 |
已知: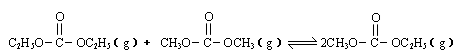 是碳酸甲乙酯的工业生产原理。下图是投料比[
是碳酸甲乙酯的工业生产原理。下图是投料比[ ]分别为3︰1和1︰1、反应物的总物质的量相同时,
]分别为3︰1和1︰1、反应物的总物质的量相同时, 的平衡转化率与温度的关系曲线。下列说法正确的是
的平衡转化率与温度的关系曲线。下列说法正确的是
| A.曲线b所对应的投料比为3︰1 |
| B.M点对应的平衡常数小于Q点 |
| C.N点对应的平衡混合气中碳酸甲乙酯的物质的量分数为0.58 |
| D.M点和Q点对应的平衡混合气体的总物质的量之比为2︰1 |
一定温度下,在一固定体积的容器中,通人一定量的CO和H2O,发生如下反应:CO(g)十H2O(g) CO2(g)十H2 (g) △H<0。在850℃时,CO和H2O浓度变化如下左图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。下列说法正确的是:
CO2(g)十H2 (g) △H<0。在850℃时,CO和H2O浓度变化如下左图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。下列说法正确的是:
| A.850℃时,按左图所示0~4min用CO2表示的平均反应速率v(CO2)=0.02mol·L-1·min-1 |
| B.t1℃高于850℃ |
| C.t1℃时,反应在4min~5min间,平衡向逆反应方向移动,若其它条件不变,可能的原因是增大压强 |
| D.若t2℃时,各物质的平衡浓度符合c(CO2)·c(H2)=2 [c(CO)·c(H2O)],则t2℃高于850℃ |
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是

A.图①表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| B.图②表示向乙酸溶液中通入氨气至过量的过程,溶液导电性的变化 |
| C.图③表示在1 L 1 mol/L FeBr2溶液中通入Cl2时Br-的量的变化 |
| D.图④表示一定浓度Na2CO3溶液中滴加盐酸,生成CO2与滴加盐酸的物质的量的关系 |
在某化学反应中,生成物B的浓度在10 s内从1.5 mol/L变成2.0 mol/L,则这10 s内B的平均反应速率是
| A.0.05 mol/(L·s) | B.0.05 mol/L |
| C.0.20 mol/(L·s) | D.0.20 mol/L |
 2C(g),经60 s达到平衡,生成0.6 mol C。下列说法正确的是
2C(g),经60 s达到平衡,生成0.6 mol C。下列说法正确的是 B(g)+C(g);ΔH ="-48.25" kJ · mol-1反应过程中时间t与A 、B浓度有下图所示关系,若测得第15min时c(B)="1.6" mol·L-1,则下列结论正确的是
B(g)+C(g);ΔH ="-48.25" kJ · mol-1反应过程中时间t与A 、B浓度有下图所示关系,若测得第15min时c(B)="1.6" mol·L-1,则下列结论正确的是
