题目内容
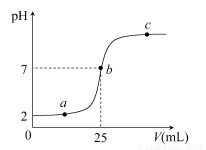
对于常温下pH均为4的三种溶液:①盐酸,②CH3COOH溶液,③NH4Cl溶液,下列说法中正确的是 ( )
A.溶液中由水电离出的c(H+):②>③
B.稀释100倍后溶液的pH:①<③
C.中和相同体积的上述溶液消耗NaOH溶液的体积:①<②
D.②和③等体积混合后的溶液:c(CH3COO-)+c(Cl-)=c(NH)
C
【解析】②抑制水的电离,③促进水的电离,故由水电离出的c(H+):③>②,A错;稀释100倍后,③中NH4+水解程度增大,酸性:③>①,pH:①>③,B错;pH相等时物质的量浓度①<②,故中和相同体积的题述溶液消耗NaOH溶液的体积:①<②,C对;②③混合溶液中根据电荷守恒:c(CH3COO-)+c(Cl-)+c(OH-)=c(NH4+)+c(H+),由于②和③溶液的pH均为4,混合后溶液不可能呈中性,则D错。

由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各界的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
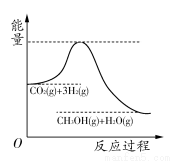
(1)上述反应平衡常数K的表达式为________,温度降低,平衡常数K________(填“增大”、“不变”或“减小”)。
(2)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。从反应开始到5 min末,用氢气浓度变化表示的平均反应速率v(H2)=________。
t/min | 0 | 2 | 5 | 10 | 15 |
n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
(3)在相同温度容积不变的条件下,能说明该反应已达平衡状态的是________(填写序号字母)。
a.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
b.容器内压强保持不变
c.H2的消耗速率与CH3OH的消耗速率之比为3∶1
d.容器内的密度保持不变
(4)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是________(填写序号字母)。
a.及时分离出CH3OH气体
b.适当升高温度
c.保持容器的容积不变,再充入1 mol CO2和3 mol H2
d.选择高效的催化剂