题目内容
【题目】(1)基态Cu原子的核外电子排布式为____________________
(2)从原子轨道重叠方式考虑,氮分子中的共价键类型有____________;
(3)![]() 水溶液中
水溶液中
①水分子中氧原子的杂化类型是_____,![]() 键键角____
键键角____![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]()
②不存在的微粒间作用力有______ 。
A.离子键 ![]() 极性键
极性键 ![]() 配位键
配位键 ![]() 氢键
氢键 ![]() 范德华力
范德华力
(4)黄铜矿冶炼铜时产生的![]() 可经过
可经过![]() 途径形成酸雨。
途径形成酸雨。
①![]() 的空间构型为________。从结构角度,解释
的空间构型为________。从结构角度,解释![]() 的酸性强于
的酸性强于![]() 的原因是_______
的原因是_______
②已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域![]() 键”
键”![]() 或大
或大![]() 键
键![]() 。大
。大![]() 键可用
键可用![]() 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大![]() 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大![]() 键表示为
键表示为![]() 。下列微粒中存在“离域
。下列微粒中存在“离域![]() 键”的是_____;
键”的是_____;
A.![]() B.
B.![]() C.
C.![]()
③铜晶体中Cu原子的堆积方式如图①所示,其堆积方式为_____,配位数为_______.
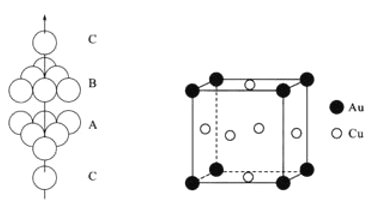
④金铜合金的晶胞如图②所示。金铜合金具有储氢功能,储氢后Au原子位于顶点,Cu原子位于面心,H原子填充在由1个Au原子和距Au原子最近的3个Cu原子构成的四面体空隙中,若Cu原子与Au原子的最短距离为![]() ,阿伏加德罗常数的位为
,阿伏加德罗常数的位为![]() ,则该晶体储氢后密度为______
,则该晶体储氢后密度为______![]() 列出计算式
列出计算式![]() 。
。
【答案】![]()
![]() 键和
键和![]() 键
键 ![]()
![]()
![]()
![]() 型 硫酸中含有的非羟基氧更多
型 硫酸中含有的非羟基氧更多![]() 非羟基氧的数目越多,中心原子带的正电荷就越多,对羟基氧的吸引力就越强,削弱了羟基
非羟基氧的数目越多,中心原子带的正电荷就越多,对羟基氧的吸引力就越强,削弱了羟基![]() 键,使氢很容易电离。
键,使氢很容易电离。![]()
![]() 面心立方最密堆积 12
面心立方最密堆积 12 ![]() 或
或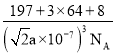 也可以
也可以![]()
【解析】
![]() 基态Cu原子的核外电子排布式为
基态Cu原子的核外电子排布式为![]() ,注意铜原子的特殊性;
,注意铜原子的特殊性;
![]() 从原子轨道重叠方式考虑,氮分子中的共价键类型有
从原子轨道重叠方式考虑,氮分子中的共价键类型有![]() 键和
键和![]() 键;
键;
![]() 水溶液中水分子中氧原子的杂化类型是
水溶液中水分子中氧原子的杂化类型是![]() ;由于分子中含有2对孤对电子,所以在斥力的影响下
;由于分子中含有2对孤对电子,所以在斥力的影响下![]() 键键角
键键角![]() ;
;
![]() 水溶液中KCl完全电离成离子,不存在离子键,水分子中含有极性键,水分子之间存在氢键和范德华力,
水溶液中KCl完全电离成离子,不存在离子键,水分子中含有极性键,水分子之间存在氢键和范德华力,![]() 存在配位键,所以不存在的微粒间作用力是离子键,答案选A;
存在配位键,所以不存在的微粒间作用力是离子键,答案选A;
![]() 黄铜矿冶炼铜时产生的
黄铜矿冶炼铜时产生的![]() 可经过
可经过![]() 途径形成酸雨。
途径形成酸雨。![]() 的空间构型为V型;从结构角度,解释
的空间构型为V型;从结构角度,解释![]() 的酸性强于
的酸性强于![]() 的原因是硫酸中含有的非羟基氧更多(非羟基氧的数目越多,中心原子带的正电荷就越多,对羟基氧的吸引力就越强,削弱了羟基
的原因是硫酸中含有的非羟基氧更多(非羟基氧的数目越多,中心原子带的正电荷就越多,对羟基氧的吸引力就越强,削弱了羟基![]() 键,使氢很容易电离。);
键,使氢很容易电离。);
![]() 已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域
已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域![]() 键”
键”![]() 或大
或大![]() 键
键![]() 。大
。大![]() 键可用
键可用![]() 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大![]() 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大![]() 键表示为
键表示为![]() 。下列微粒中存在“离域
。下列微粒中存在“离域![]() 键”的是
键”的是![]() 、
、 ![]() ;
;
故答案为AB;
![]() 铜晶体中Cu原子的堆积方式如图
铜晶体中Cu原子的堆积方式如图![]() 所示,其堆积方式为面心立方最密堆积;配位数为12;
所示,其堆积方式为面心立方最密堆积;配位数为12;
![]() 金铜合金的晶胞如图
金铜合金的晶胞如图![]() 所示。金铜合金具有储氢功能,储氢后Au原子位于顶点,Cu原子位于面心,H原子填充在由1个Au原子和距Au原子最近的3个Cu原子构成的四面体空隙中,若Cu原子与Au原子的最短距离为
所示。金铜合金具有储氢功能,储氢后Au原子位于顶点,Cu原子位于面心,H原子填充在由1个Au原子和距Au原子最近的3个Cu原子构成的四面体空隙中,若Cu原子与Au原子的最短距离为![]() ,阿伏加德罗常数的位为
,阿伏加德罗常数的位为![]() ,则该晶体储氢后密度为
,则该晶体储氢后密度为![]() (或
(或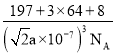 也可以)
也可以)![]() 。
。

 优百分课时互动系列答案
优百分课时互动系列答案【题目】根据杂化轨道理论和价电子对互斥理论模型判断,下列分子或离子的中心原子的杂化方式及空间构型正确的是( )
选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥理论模型 | 分子或离子的空间构型 |
A |
|
| 直线形 | 直线形 |
B |
|
| 平面三角形 | 三角锥形 |
C |
|
| 四面体形 | 平面三角形 |
D |
|
| 四面体形 | 正四面体形 |
A.AB.BC.CD.D
【题目】高炉炼铁过程中发生反应: ![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g),该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
Fe(s)+CO2(g),该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
温度T/℃ | 1000 | 1150 | 1300 |
平衡常数K | 4.0 | 3.7 | 3.5 |
A. 由表中数据可判断该反应:反应物的总能量<生成物的总能量
B. 1000℃下Fe2O3与CO反应,t min达到平衡时c(CO) =2×10-3 mol/L,则用CO2表示该反应的平均速率为2×10-3/t mol·L-1·min-1
C. 为了使该反应的K增大,可以在其他条件不变时,增大c(CO)
D. 其他条件不变时,增加Fe2O3的用量,不能有效降低炼铁尾气中CO的含量
