题目内容
8.(1)在NaCl晶体中,离Na+距离最近的Cl-有6个(2)在晶体硅中,硅原子与Si-Si(硅硅共价键)个数比为1:2
(3)按要求填空
①HClO电子式
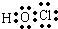
②二氧化碳的结构式O=C=O
③砹的分子式At2
④CCl4的空间构型为正四面体
⑤S原子结构示意图
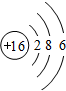
⑥用电子式表示K2S的形成过程
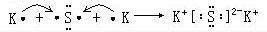 .
.
分析 (1)根据氯化钠的晶胞图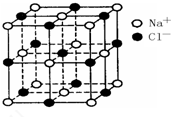 分析;
分析;
(2)晶体硅中每个Si原子形成4个共价键,每个共价键由2个原子构成;
(3)①HClO为共价化合物,分子中存在1个H-O键和1个Cl-O键;
②二氧化碳中存在2个碳氧双键;
③砹与碘为同主族元素,都是双原子分子;
④CCl4的空间构型与甲烷相同;
⑤S原子核内有16个质子,核外有16个电子;
⑥K2S为离子化合物,离子化合物阴离子带电荷且用“[]”,共价化合物不带电荷,注意各原子或离子满足稳定结构.
解答 解:(1)由氯化钠的晶胞图 可以看出,与每个Na+距离最近且相等的Cl-共有6个;
可以看出,与每个Na+距离最近且相等的Cl-共有6个;
故答案为:6;
(2)晶体硅中每个Si原子形成4个Si-Si共价键,每个共价键由2个原子构成,则硅原子与Si-Si(硅硅共价键)个数比为1:2;
故答案为:1:2;
(3)①HClO为共价化合物,分子中存在1个H-O键和1个Cl-O键,次氯酸的电子式为: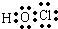 ;
;
故答案为: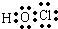 ;
;
②二氧化碳中存在2个碳氧双键,其结构式为O=C=O;
故答案为:O=C=O;
③砹与碘为同主族元素,都是双原子分子,其分子式为At2;
故答案为:At2;
④CCl4的空间构型与甲烷相同,为正四面体结构;
故答案为:正四面体;
⑤S原子核内有16个质子,核外有16个电子,分三层排布,其原子结构示意图为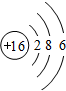 ;
;
故答案为: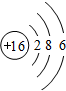 ;
;
⑥K2S为离子化合物,用电子式表示形成过程为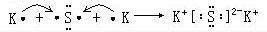 ,
,
故答案为: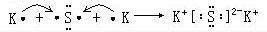 .
.
点评 本题是一道综合知识的考查题目,涉及晶胞的结构、原子结构、电子式、结构式、原子结构示意图,要求学生具有分析和解决问题的能力,注意平时知识的积累是解题的关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列操作中错误的是( )
| A. | 提取溶解在水中的少量碘:加入CCl4,振荡、静置分层后,取出有机层再分离 | |
| B. | 除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层 | |
| C. | 除去CO2中的少量SO2;通过盛有饱和NaHCO3溶液的洗气瓶 | |
| D. | 除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯 |
19.已知,室温下存在反应3HNO2═HNO3+2NO↑+H2O;在酸性溶液中,NO 可将 MnO还原为Mn2+且无气体生成;酸性KMnO4溶液可吸收氮的氧化物.某化学兴趣小组设计了如下探究实验(实验前先排尽装置中的空气):
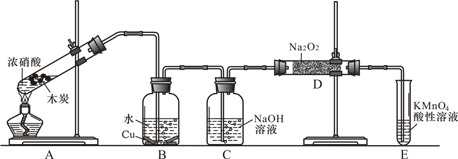
请回答下列问题:
(1)装置A的试管中发生反应的化学方程式是C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B瓶中可以观察到的现象是产生无色气体,溶液逐渐变蓝,C瓶出来的气体是NO.
(3)实验时观察到D 管内固体颜色逐渐变为白色.据此甲同学认为D管中生成物是NaNO3,而乙同学则认为D管中生成的是NaNO2,如何证明乙同学的观点正确?
(4)E装置的作用是吸收D中未反应完的NO,以免污染空气.
(5)同学们经讨论认为上述装置仍有缺陷,为了避免D管中生成NaOH,你认为应该进行的改进是在C、D之间增加一个盛浓硫酸的洗气瓶(或装无水CaCl2的干燥管).

请回答下列问题:
(1)装置A的试管中发生反应的化学方程式是C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B瓶中可以观察到的现象是产生无色气体,溶液逐渐变蓝,C瓶出来的气体是NO.
(3)实验时观察到D 管内固体颜色逐渐变为白色.据此甲同学认为D管中生成物是NaNO3,而乙同学则认为D管中生成的是NaNO2,如何证明乙同学的观点正确?
| 实验操作 | 实验现象 | 实验结论 |
| D管生成的是NaNO2 |
(5)同学们经讨论认为上述装置仍有缺陷,为了避免D管中生成NaOH,你认为应该进行的改进是在C、D之间增加一个盛浓硫酸的洗气瓶(或装无水CaCl2的干燥管).
13.物质的量相等的下列烃,在相同条件下完全燃烧,耗氧量最多的是( )
| A. | C2H6 | B. | C3H6 | C. | C4H6 | D. | C7H16 |
17.下面的能级表示中正确的是( )
| A. | 1p | B. | 2d | C. | 3f | D. | 4s |
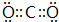 .
.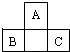 A、B、C为短周期元素,它们的位置关系如图所示,已知B、C两元素原子序数之和是A元素的原子序数的4倍,则A、B、C的元素符号分别:
A、B、C为短周期元素,它们的位置关系如图所示,已知B、C两元素原子序数之和是A元素的原子序数的4倍,则A、B、C的元素符号分别: ,B在周期表中的位置第三周期第VA族,C的离子结构示意图为
,B在周期表中的位置第三周期第VA族,C的离子结构示意图为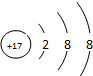 ,A的氢化物分子式为H2O;B、C的最高价氧化物水化物的分子式分别为H3PO4、HClO4,它们的酸性HClO4比H3PO4强.
,A的氢化物分子式为H2O;B、C的最高价氧化物水化物的分子式分别为H3PO4、HClO4,它们的酸性HClO4比H3PO4强.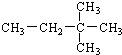 2,2-二甲基-丁烷
2,2-二甲基-丁烷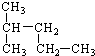 2-甲基-戊烷.
2-甲基-戊烷.